
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




STAT3是一種在多種組織中表達的信號分子,調控一係列與癌細胞生長、增殖、血管生成、轉移、耐藥性和免疫逃逸等有關的基因。因此,靶向 STAT3 信號通路已成為許多癌症的潛在治療策略。hjc黄金城可以為客戶提供STAT3藥物發現、藥學研究(原料藥工藝開發+製劑)、臨床前研究服務(包括藥效、藥代、安評)以及IND申報等一站式服務。
信號轉導和轉錄激活因子(signal transducer and activator of transcription, STAT)是一大類具有細胞質內信號轉導和細胞核內轉錄激活雙重作用的蛋白,廣泛存在於哺乳動物細胞中,介導多種細胞內信號通路。盡管STAT家族成員高度同源,但功能卻千差萬別。
STAT3是一種在多種組織中表達的信號分子。STAT3可被多種因素激活,包括細胞因子、生長因子、神經內分泌因素、缺血缺氧刺激等。作為一種功能多樣化的轉錄因子,STAT3能與大量的信號分子相互作用,並形成了多種細胞內外信號通路。
STAT3參與了細胞的增殖、存活、分化和血管生成等多種生物學過程。在正常細胞中,STAT3通過磷酸化瞬時激活,將質膜上的細胞因子和生長因子受體的轉錄信號傳遞到細胞核。研究表明,持續激活的STAT3對於多種癌症是必不可少的,比如乳腺癌和結直腸癌,這使得STAT3成為理想的藥物靶點。然而,STAT3在大多數人類癌症中變得過度激活,通常與不良的臨床預後有關。
STAT3通過信號轉導和轉錄激活參與了生物體內複雜多樣的生命活動,是當前的研究熱點,其在腫瘤領域的研究已經取得階段性的成果,STAT3作為多種腫瘤通路的匯合點,在腫瘤細胞中持續大量表達,能夠促進腫瘤細胞增殖、抵抗細胞凋亡、介導原癌性炎症和抑製抗腫瘤免疫等,STAT3在一定程度上已經成為腫瘤治療的重要分子靶點!
STAT家族由七個成員組成,即STAT1、STAT2、STAT3、STAT4、STAT5A、STAT5B和STAT6。STAT3有兩種具有不同功能的剪接亞型,STAT3α和STAT3β。STAT3α的結構域完整,STAT3β與STAT3α相比在C末端缺失55個氨基酸殘基。STAT3β比STAT3α具有更好的特異性DNA結合活性。STAT3的主要作用是促進腫瘤生長和免疫抑製。編碼STAT3的基因位於人類17號染色體上,該蛋白質由770個氨基酸組成,具有六個功能保守結構域:
❖ N末端結構域(NTD):促進STAT二聚體的形成,使其隨後能夠與轉錄因子結合;
❖ 螺旋卷曲結構域(CCD),用於向受體招募STAT3以及隨後的磷酸化、二聚化和核轉位;
❖ DNA結合結構域(DBD),用於識別和結合靶基因調控區域的DNA序列;
❖ 連接結構域(LD),將DBD連接到SH2域,確保DNA結構域的穩定性;
❖ SRC同源2結構域(SH2):最高度保守的STAT結構域,用於招募和激活STAT3分子,通過與相對亞基中的磷酸化酪氨酸殘基相互作用來實現STAT3分子的二聚化;
❖ 轉錄激活結構域(TAD):通過磷酸化來促進其他轉錄激活因子的組裝。
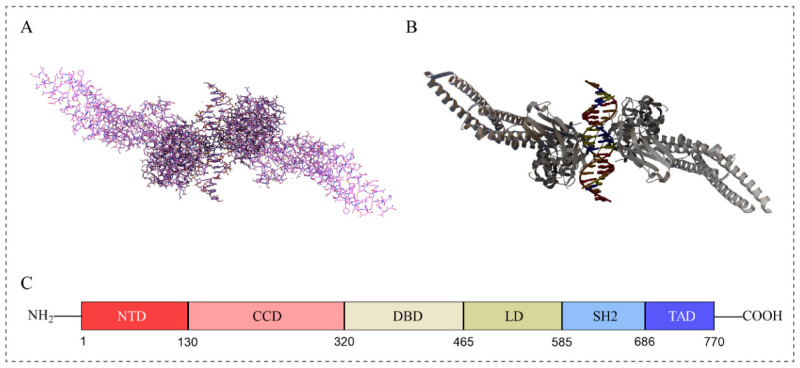
STAT3的結構示意圖[1]
JAK/STAT通路是調節細胞功能最重要的信號通路之一,該通路中已鑒定出數十種細胞因子和生長因子,包括白細胞介素(IL)、幹擾素和血管生成因子。IL-6是一種炎症介質,在腫瘤微環境(TME) 中,IL-6可由多種細胞產生,包括巨噬細胞、中性粒細胞、成纖維細胞和腫瘤細胞本身。IL-6可以直接引起癌細胞增殖,還可以促進TME中其他炎症因子的產生,並招募大量免疫細胞。因此,IL-6是慢性炎症和腫瘤進展的關鍵物質。響應IL-6刺激,JAK/STAT3通路被磷酸化,在人體內形成關鍵的IL-6/JAK/STAT3通路,參與類風濕關節炎、炎症性腸病及許多人類癌症的過程。目前,已鑒定出四個關鍵的JAK分子,即JAK1、JAK2、JAK3和TYK2。其中,JAK3僅在造血和淋巴係統的細胞中表達,而其餘三種幾乎在所有細胞中表達。JAK包含七個同源結構域 (JH1-7),並形成四個結構域:JH1、JH2、SH2 和 FERM。
經典的IL-6信號通路由IL-6與膜結合受體IL-6受體 α (IL-6Rα) 和gp130介導,形成IL-6/IL-6R/gp130複合物,從而導致細胞內JAK激活。JAK蛋白與gp130的胞內結構域結合,導致gp130的酪氨酸殘基磷酸化,形成STAT3結合位點。STAT3識別並與磷酸酪氨酸對接位點結合後,附著的具有活性的JAK酶導致STAT3中705位酪氨酸的磷酸化,這促使兩個磷酸化的STAT3單體發生二聚化,並且進入細胞核,從而激活多種下遊基因的轉錄。
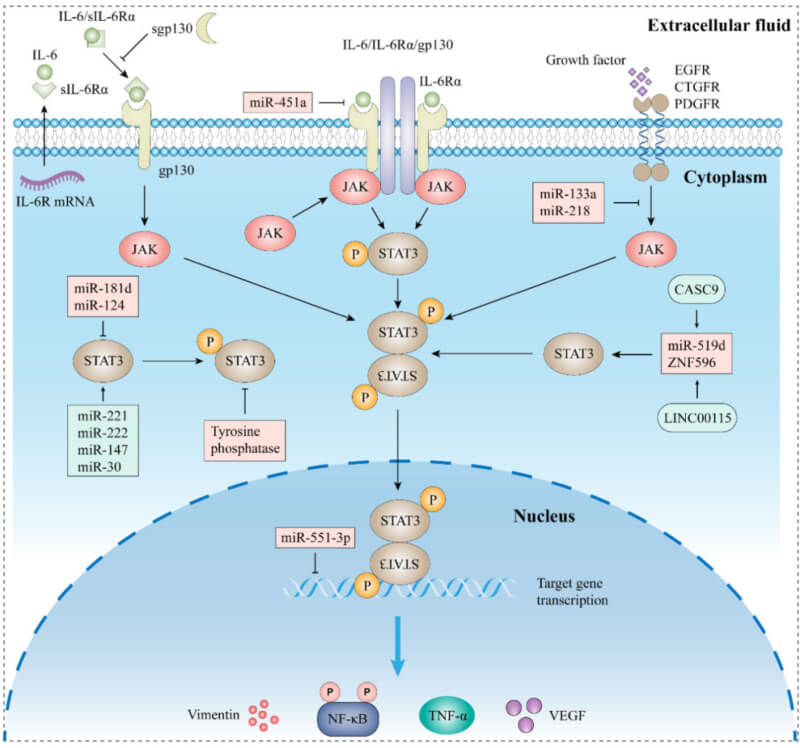
IL-6/JAK/STAT3 signaling pathway[1]
鑒於STAT3在腫瘤發生發展中的關鍵作用,以STAT3為靶點進行藥物開發已成為近二十年來主要的藥物研究熱點之一。目前已有許多化合物被報道具有STAT3相關通路抑製活性,許多藥物已進入臨床。下圖顯示了目前處於臨床研究階段的部分STAT3抑製劑,適應症包括肝癌、結直腸癌、黑色素瘤、白血病等多種疾病。
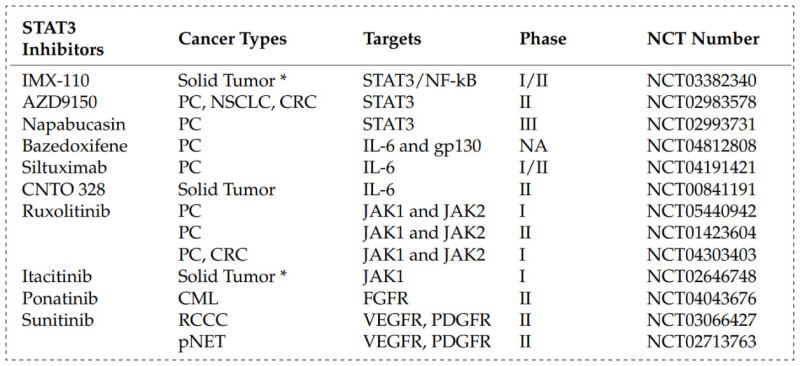
STAT3 inhibitors in clinical trials[1]
由於腫瘤發生的複雜機製,通過藥物聯用同時抑製多個靶點是一種重要的抗癌策略。目前,以化療為代表的傳統方法仍然是治療癌症的主要選擇。然而大多數化療藥物僅作用於一個靶點,治療一段時間後還可能會產生耐藥性。調節兩個或多個相關靶點的藥物可能會在癌症治療中產生協同治療效果。因此,越來越多的抑製兩個特定靶點的療法在臨床研究中取得了成功。
組蛋白去乙酰化酶(histone deacetylase,HDAC)是一類與腫瘤發生密切相關的表觀遺傳酶,在許多重要的細胞過程中起著重要的調節作用,包括細胞生長、細胞分化和細胞凋亡。多種HDAC抑製劑(HDACi)在體外對多種類型的癌細胞(包括結腸癌、乳腺癌和肝癌等)具有顯著的抗腫瘤作用。目前獲批的HDACi的適應症主要集中在血液係統惡性腫瘤,如淋巴瘤和骨髓瘤。而HDACi 對人類實體瘤缺乏明顯的功效,這限製了其在更多腫瘤適應症中的應用。
最近研究表明,HDAC的抑製將通過級聯反應導致乳腺癌中相關藥物靶點STAT3的代償性激活,這可能會限製HDAC抑製劑在實體瘤中的抗增殖作用。本研究中科研人員將HDACi藥團與其他蛋白抑製劑結合起來,設計了一係列STAT3-HDAC雙靶點抑製劑,以提高針對固體腫瘤的療效。與BRD4-HDAC和JAK1-HDAC抑製相比,STAT3-HDAC抑製可能是一種有效的替代組合。科研人員選擇STAT3抑製劑紫檀芪 (Pterostilbene,PTE) 作為母體分子。PTE是從藍莓中提取的白藜蘆醇的天然二甲基化類似物。通過將HDAC抑製劑SAHA(伏立諾他)的藥效團摻入PTE中,合成了一係列具有STAT3-HDAC雙靶點抑製活性的強效紫檀芪異羥肟酸衍生物。
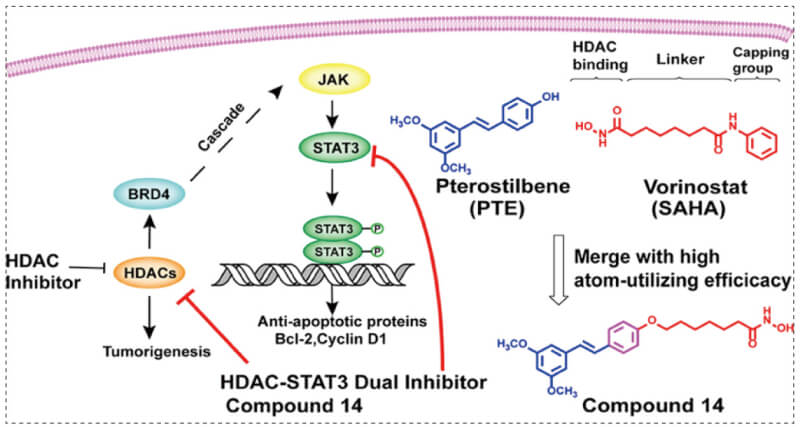
HDAC-BRD4-LIFR-JAK-STAT3 signal cascade[2]
其中,Compound 14 是一種出色的異羥肟酸酯衍生物,可直接與STAT3結合,具有強大的親和力(KD=33 nM),在體外有效抑製HDAC, IC50為23.15nM。且Compound 14在體內外具有高效的抗增殖能力,抑製MDA-MB-231細胞(IC50=0.78 μM)和 HCT116細胞(IC50= 1.07 μM)。Compound 14在體外實驗中表現出良好的抗腫瘤活性,因此研究人員建立了小鼠同種異體移植瘤模型來評價Compound 14的體內抗腫瘤活性。Compound 14在劑量15 mg/kg組與對照組相比體積減少54%,瘤重減少53%。在劑量30 mg/kg組體積減少64%,瘤重減少62%。此外Compound 14沒有引起明顯的體重變化。實驗結果表明,Compound 14具有良好的安全性,是一種很有前途的抗癌化合物。
在此項研究中,科研人員通過hjc黄金城評估了Compound 14在SD大鼠中靜脈和口服給藥的藥代動力學(PK) 數據。下圖顯示Compound 14具有出色的整體PK曲線:靜脈注射Compound 14(2 mg/kg)後,穩態(Vss)的平均分布量為1.65 L/kg。平均血清除率 (Cl)為63.89 mL/min/kg。平均半衰期(T1/2)為0.47h。口服Compound 14(20 mg/kg)後,口服生物利用度(F)平均為5.81%,平均半衰期(T1/2)為0.88h。
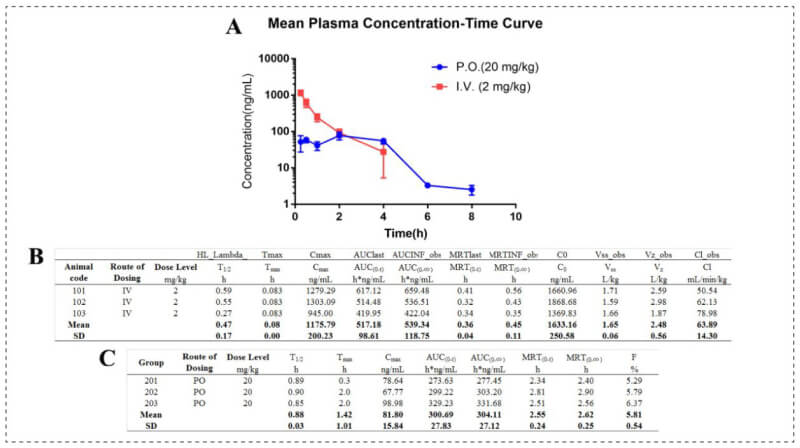
Pharmacokinetics of 14 in SD rats[2]
2023年7月,宇耀生物自主研發的STAT3雙功能磷酸化位點靶向抑製劑——YY201臨床試驗申請正式獲得NMPA批準,適應症為晚期實體瘤和複發難治性惡性血液腫瘤。宇耀生物科學家團隊一直專注於STAT3靶點的基礎和轉化研究,並借助AI技術首次發現並開發出了納摩爾級STAT3雙磷酸化位點抑製劑、全球領先的First-in-class小分子靶向藥物“YY201”。該藥物通過與STAT3直接結合,抑製STAT3的 Tyr705和Ser727雙位點磷酸化,抑製STAT3功能和阻斷下遊信號傳遞,從而發揮抑製腫瘤作用。體外藥理學和藥效學研究表明,YY201與STAT3的親和活性在1-10納摩爾,在胰腺癌、三陰性乳腺癌、肺癌、急性髓係白血病、淋巴瘤等實體腫瘤和血液腫瘤的體外增殖抑製活性在1-10 nM,在多種體內模型中表現出顯著的抗腫瘤作用,極低劑量下可致腫瘤完全消退,藥代動力學和毒理學研究亦證實YY201良好的成藥性和安全性。
hjc黄金城作為宇耀生物的合作夥伴,為YY201提供了藥學研究服務(包括原料藥、製劑)、臨床前研究服務(包括藥效、藥代、安評)以及IND申報服務等,助力YY201成功通過IND 審批進入臨床試驗階段。
相關閱讀: hjc黄金城助力宇耀生物STAT3雙磷酸化抑製劑YY201獲批臨床
作為眾多致癌信號通路的匯聚點,STAT3在調節抗腫瘤免疫反應中發揮著重要作用。STAT3在抑製關鍵的免疫激活調節因子的表達和促進免疫抑製因子的產生方麵發揮著重要作用。
目前,STAT3靶向藥物的開發已經進入深度開發階段。雖然目前市場上還沒有相關藥物,但已經凸顯出巨大的應用前景。未來會越來越重視以STAT3為靶點的藥物開發,不斷推出新的藥物開發技術,如PROTAC技術。STAT3-PROTAC既能抑製STAT3的功能,又能直接降解STAT3,在克服腫瘤耐藥性方麵有很大優勢。因此,靶向STAT3信號通路已成為治療多種癌症的一種有前途的策略!
[1] Xin Li, et al. STAT3 Inhibitors: A Novel Insight for Anticancer Therapy of Pancreatic Cancer. Biomolecules. 2022 Oct 9;12(10):1450. doi: 10.3390/biom12101450.
[2] Yuhao Ren, et al. Discovery of STAT3 and Histone Deacetylase (HDAC) Dual-Pathway Inhibitors for the Treatment of Solid Cancer. J Med Chem. 2021 Jun 10;64(11):7468-7482. doi: 10.1021/acs.jmedchem.1c00136.
[3]Sailan Zou, et al. Targeting STAT3 in Cancer Immunotherapy. Mol Cancer. 2020 Sep 24;19(1):145.DOI: 10.1186/s12943-020-01258-7
 相關新聞
相關新聞