
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com





細胞色素P450超家族(CYP450)是一大類各種各樣的酶,因在450納米有特異吸收峰而得名,其主要功能是催化氧化有機化合物。細胞色素P450在內源性(如脂肪酸、類固醇、前列腺素和膽汁酸等)和外源性物質(如藥物、環境致癌物和食品添加劑等)的代謝過程中,具有重要作用,而且是藥物代謝與生物激活作用的主要酶類,約占到各種代謝反應總數的75%。近年來,對細胞色素P450的結構、功能,特別是在藥物代謝中的作用的研究有了較大的進展,研究表明細胞色素P450是藥物代謝過程中的關鍵酶,而且對細胞因子和體溫調節都有重要影響。
細胞色素P450是由許多微粒體和線粒體亞鐵血紅素-硫酸鹽蛋白組成的,廣泛存在於細菌、真菌、植物和動物體內。1958年,這些細胞色素在肝髒細胞微粒體中被發現,哺乳動物細胞色素P450是膜的組分,參與生物合成和許多生理有效物質的代謝,除了在骨骼肌和成熟紅血球之外所有的器官和組織中都有發現。到目前為止,已測序和命名了三千多個細胞色素P450基因。根據氨基酸序列的同源性,細胞色素P450超家族成員依次分為家族、亞家族和酶個體三個級別。
CYP1B1的相關內容
細胞色素P450構成了參與多種內源性和外源性化合物代謝的血紅素蛋白的基本家族。人類細胞色素P450的基因也已經基本明確,包括57個活性基因和58個假基因,分為18個家族和44個亞家族。其中,涉及藥物代謝的CYP450主要包括CYP1、CYP2和CYP3家族,參與大量外源性化學物質和某些內源性物質的代謝。
CYP1家族屬於人類已知的18個CYP基因家族,包括三種酶:CYP1A1,CYP1A2和CYP1B1。CYP1B1基因位於2號染色體上,有三個外顯因子和兩個內含子,編碼一個由543個氨基酸所組成的酶蛋白。
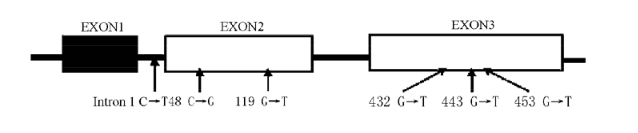
人體內的CYP1B1與CYP1A1和CYP1A2分別具有41%和40%的氨基酸序列同源性,而後兩者具有72%的同源性。CYP1B1是上述三種CYP1中最有趣的靶標,因為CYP1B1是催化強效雌激素C18-類固醇17b-雌二醇(E2)羥化的最有效酶。
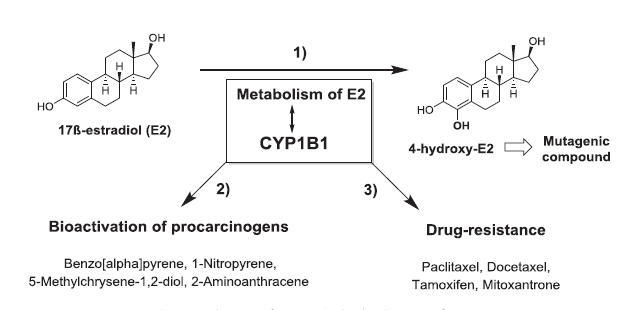
CYP1B1能氧化代謝許多前致癌物(如催化多環芳香烴和芳香胺的活化)和體內的甾體激素(如介導17-雌二醇羥化,形成4-兒茶酚雌激素)。與CYP1A1、1A2等相比,CYP1B1催化雌二醇4-羥化活性最高,是4-羥化代謝的主要酶。
CYP1B1抑製劑的研究方向
抑製細胞色素P450 1B1(CYP1B1)是一種很有前途的生物標誌物和治療靶點,因為它可以在三個不同的水平上起作用:
(1)通過抑製誘變性4-羥基雌二醇的形成;
(2)通過抑製前致癌物的生物活化;
(3)通過降低耐藥性。
根據藥物代謝能力的不同,臨床病人共有四種代謝表型。分別是超強代謝型:攜帶3個或更多個功能正常的野生型等位基因,在人群中占1%~10%;這類人群若給予標準劑量,則不能獲得預期的效果,必須適當增加劑量。強代謝型:由兩個野生型或兩個功能正常的等位基因編碼的酶活性正常表型,占人群的75%~85%,這類人群在標準劑量時即有較好的療效。中間代謝型:攜帶一個野生型和一個變異型等位基因;或一個有活性、一個無活性;或一個無活性、一個有部分活性的基因編碼的代謝酶,功能略有減弱,占人群的10%~15%。弱代謝型:攜帶有兩個變異等位基因而使酶活性降低或缺失,占人群的5%~10%。這類人群因代謝受阻,藥物易蓄積體內而引發中毒,故必須適當減量或更換其他藥物。
CYP1B1在幾種類型的癌症中都存在過表達,並與耐藥性有關。目前已經進行了幾項研究以開發CYP1B1的有效和選擇性抑製劑,研究報道中的CYP1B1抑製劑包括:類黃酮,反式二苯乙烯,香豆素,生物堿,蒽醌和其他幾種化合物[1]。在這些化合物家族中,類黃酮和芪類素研究最多;而二苯乙烯家族在活性和選擇性方麵提供了最好的抑製劑,特別是2,4,3,5-四甲氧基二苯乙烯,它是CYP1B1最具選擇性的抑製劑之一[2]。
二苯乙烯類:二苯乙烯的基本結構是在雙鍵的兩側具有兩個芳族基團。白藜蘆醇存在於紅葡萄酒中,具有抗氧化活性,白藜蘆醇對CYP1B1有抑製作用但卻沒有選擇性,因為它也抑製CYP1A1 [3]。而作為二苯乙烯類的化合物9是CYP1B1的高效和高選擇性抑製劑。
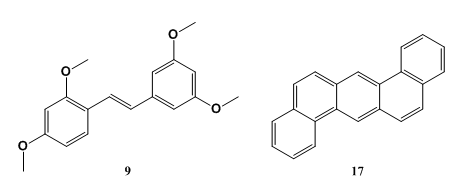
多環芳香族化合物:多環芳族化合物長期以來被認為是CYP1酶的抑製劑,其中化合物17是CYP1B1的有效地和有選擇性地抑製。
黃酮類化合物:黃酮類化合物是我們飲食中抗氧化劑的主要來源[4],而且類黃酮具有良好的抗癌特性。
香豆素:香豆素構成一類衍生自香豆素的酚類化合物,也稱為2H-1-苯並二氫吡喃-2-酮。這些天然存在的化學物質具有作為化學抑製劑的潛力,並且已知一些化學物質與CYP1酶相互作用,且CYP1B1的抑製活性根據酶底物的變化而發生變化。
蒽醌類:蒽醌類是指一組衍生自蒽醌的分子,蒽醌本身是蒽的衍生物。蒽醌是在一些動物和植物中發現的多環芳烴。在這類化合物中報道的兩種CYP1B1抑製劑是紫紅素和茜素,Ki值分別為0.7和0.5mM。
天然生物堿:生物堿構成各種氮化合物的家族,通常是雜環,並且它們主要存在於植物中。化合物64是有效的CYP1B1抑製劑。
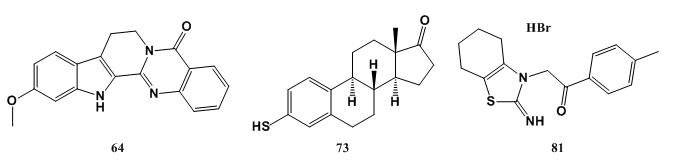
其他化合物:最近報道化合物73是從90種類固醇衍生物進行的篩選中鑒定的最佳CYP1B1抑製劑(IC50 = 3.4mM)[5]。另一個是化合物81,一種抑製p53基因(人體抑癌基因)激活和凋亡的化合物,而且已經觀察到該化合物直接影響CYP1酶的催化活性,並且是CYP1B1的非常有效的抑製劑[6]。
除了已知的CYP1B1抑製劑的改進和新抑製劑的開發之外,使用上述這些結構數據的分子建模研究可以指導有效和有選擇性CYP1B1抑製劑的合成。
關於CYP1B1抑製劑的新進展
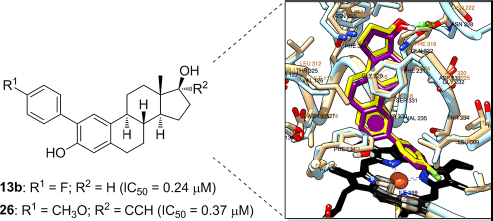
CYP1B1過表達在不同類型的人類癌症中觀察到,例如乳腺癌,肺癌,食道癌,皮膚癌,睾丸癌,結腸癌,淋巴結癌和腦癌。Raphael Dutour等[7]合成了四個係列的類固醇衍生物,來評估它們對CYP1B1和CYP1A1的抑製活性及選擇性。四個係列分別為:(1) 12 estrone (E1)-and 17β-estradiol (E2)-derivatives bearing a3-or a 4-pyridinyl core at C2, C3, or C4, (2) eight estrane derivatives withdifferent sulfur groups at C3, (3) 19 E1-and E2¬derivatives bearing distinctaryls at C2, and (4) five D-ring derivatives. 這些類固醇衍生物都有較高的合成產率,並通過IR,1H NMR,13C NMR和HRMS等分析方法進行了充分的表征。
該係列的最有效的CYP1B1抑製劑是化合物13b和20b,分別帶有4-氟苯基和4-甲氧基苯基,而化合物26具有較好的CYP1B1抑製活性。
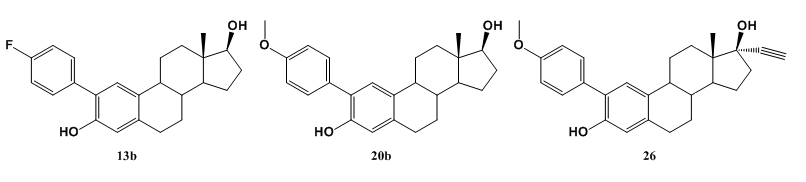
結果表明,與CYP1A1相比,這些新的類固醇衍生物能更好地進入CYP1B1結合位點,對CYP1B1有較好的選擇性。
年齡、種族、身體狀況、基因和環境的多種因素的差異會對藥物代謝有不同的影響,因此不同的病人對同一種藥物在藥物代謝方麵會有差異。CYP450是人體參與藥物代謝最重要的一種酶,越來越多的研究已經證實,CYP450基因的多態性是造成臨床不同個體間藥物代謝差異的主要原因之一。近十多年來,我們在CYP450藥物基因組學研究方麵取得了很大的進展。但是我們也應該清醒地認識到,個體化用藥在國內的發展還存在很多問題,要想在臨床上真正實現個體化用藥,還有很長的路要走。
參考文獻:
[1], Raphael Dutour, Donald Poirier. Inhibitors ofcytochrome P450 (CYP) 1B1.European Journal of MedicinalChemistry 135 (2017) 296-306.
[2] Y.J. Chun, S. Kim, D. Kim, S.K. Lee, F.P. Guengerich.A new selective and potent inhibitor of human cytochrome P450 1B1 and itsapplication to antimuta¬genesis, Cancer Res. 61 (2001) 8164e8170.
[3] T.K. Chang, W.B. Lee, H.H. Ko. Trans-resveratrolmodulates the catalytic ac¬tivity and mRNA expression of the procarcinogen-activatinghuman cyto¬chrome P450 1B1, Can. J. Physiol. Pharm. 78 (2000) 874e881.
[4] F. Ververidis, E. Trantas, C. Douglas, G. Vollmer,G. Kretzschmar, N. Panopoulos. Biotechnology of flavonoids and otherphenylpropanoid¬derived natural products. Part I: chemical diversity, impactson plant biology and human health, Biotechnol. J. 2 (2007) 1214e1234.
[5] D. Poirier, J. Roy, F. Cortez-Benitez, R. Dutour.Targeting cytochrome P450 (CYP) 1B1 with steroid derivatives, Bioorg. Med.Chem. Lett. 26 (2016) 5272e5276.
[6] L. Sparfel, J. Van Grevenynghe, M. Le Vee, C.Aninat, O. Fardel. Potent inhibition of carcinogen-bioactivating cytochrome P4501B1 by the p53 inhibitor pifi-thrin alpha, Carcinogenesis 27 (2006) 656e663.
[7] Raphael Dutour, Jenny Roy, FranciscoCortés-Benítez, Reneb Maltais, and Donald Poirier. Targeting Cytochrome P450(CYP) 1B1 Enzyme with Four Series of A Ring Substituted Estrane Derivatives:Design, Synthesis, Inhibitory Activity, and Selectivity. J. Med. Chem. 2018,61, 9229−9245.
 相關新聞
相關新聞