一、ELISA的原理
ELISA的基礎是抗原或抗體的固相化及抗原或抗體的酶標記。結合在固相載體表麵的抗原或抗體仍保持其免疫學活性,酶標記的抗原或抗體既保留其免疫學活性,又保留酶的活性。在測定時,受檢標本(測定其中的抗體或抗原)與固相載體表麵的抗原或抗體起反應。用洗滌的方法使固相載體上形成的抗原抗體複合物與液體中的其他物質分開。再加入酶標記的抗原或抗體,也通過反應而結合在固相載體上。此時固相上的酶量與標本中受檢物質的量呈一定的比例。加入酶反應的底物後,底物被酶催化成為有色產物,產物的量與標本中受檢物質的量直接相關,故可根據呈色的深淺進行定性或定量分析。由於酶的催化效率很高,間接地放大了免疫反應的結果,使測定方法達到很高的敏感度。
二、ELISA的類型
ELISA可用於測定抗原,也可用於測定抗體。在這種測定方法中有三個必要的試劑:
(1)固相的抗原或抗體,即"免疫吸附劑"(immunosorbent);
(2)酶標記的抗原或抗體,稱為“酶聯物”、“結合物”(conjugate);
(3)酶反應的底物。根據試劑的來源和標本的情況以及檢測的具體條件,可設計出各種不同類型的檢測方法。用於臨床檢驗的ELISA主要有以下幾種類型:
(一) 雙抗體夾心法測抗原
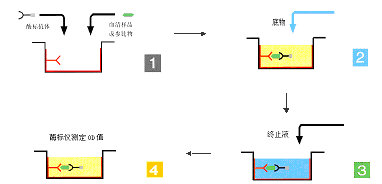
雙抗體夾心法是檢測抗原最常用的方法,操作步驟如下:
(1) 將特異性抗體與固相載體聯結,形成固相抗體。洗滌除去未結合的抗體及雜質。
(2) 加受檢標本,保溫反應。標本中的抗原與固相抗體結合,形成固相抗原抗體複合物。洗滌除去其他未結合物質。
(3) 加酶標抗體,保溫反應。固相免疫複合物上的抗原與酶標抗體結合。徹底洗滌未結合的酶標抗體。此時固相載體上帶有的酶量與標本中受檢抗原的量相關。
(4) 加底物顯色。固相上的酶催化底物成為有色產物。通過比色,測知標本中抗原的量。
在臨床檢驗中,此法適用於檢驗各種蛋白質等大分子抗原,例如HBsAg、HBeAg、AFP、hCG等。隻要獲得針對受檢抗原的異性抗體,就可用於包被固相載體和製備酶結合物而建立此法。如抗體的來源為抗血清,包被和酶標用的抗體最好分別取自不同種屬的動物。如應用單克隆抗體,一般選擇兩個針對抗原上不同決定簇的單抗,分別用於包被固相載體和製備酶結合物。這種雙位點夾心法具有很高的特異性,而且可以將受檢標本和酶標抗體一起保溫反應,作一步法檢測。
在一步法測定中,當標本中受檢抗原的含量很高時,過量抗原分別和固相抗體及酶標抗體結合,而不再形成"夾心複合物"。類同於沉澱反應中抗原過剩的後帶現象,此時反應後顯色的吸光值(位於抗原過剩帶上)與標準曲線(位於抗體過剩帶上)某一抗原濃度的吸光值相同,如按常法測讀,所得結果將低於實際的含量,這種現象被稱為鉤狀效應(hook effect),因為標準曲線到達高峰後呈鉤狀彎落。鉤狀效應嚴重時,反應甚至可不顯色而出現假陰性結果。因此在使用一步法試劑測定標本中含量可異常增高的物質(例如血清中HBsAg、AFP和尿液hCG等)時,應注意可測範圍的最高值。用高親和力的單克隆抗體製備此類試劑可削弱鉤狀效應。
假使在被測分子的不同位點上含有多個相同的決定簇,例如HBsAg的a決定簇,也可用針對此決定的同一單抗分別包被固相和製備酶結合物。但在HBsAg的檢測中應注意亞型問題,HBsAg有adr、adw、ayr、ayw4個亞型,顯然每種亞型均有相同的a決定簇的反應性,這也是用單抗作夾心法應注意的問題。
雙抗體夾心法測抗原的另一注意點是類風濕因子(RF)的幹擾。RF是一種自身抗體,多為IgM型,能和多種動物IgG的Fc段結合。用作雙抗體夾心法檢測的血清標本中如含有RF,它可充當抗原成份,同時與固相抗體和酶標抗體結合,表現出假陽性反應。采用F(ab')或Fab片段作酶結合物的試劑,由於去除了Fc段,從而可消除RF的幹擾。雙抗體夾心法ELISA試劑是否受RF的影響,已被列為這類試劑的一項考核指標。
雙抗體夾心法適用於測定二價或二價以上的大分子抗原,但不適用於測定半抗原及小分子單價抗原,因其不能形成兩位點夾心。
(二)雙抗原夾心法測抗體
反應模式與雙抗體夾心法類似。用特異性抗原進行包被和製備酶結合物,以檢測相應的抗體。與間接法測抗體的不同之處為以酶標抗原代替酶標抗抗體。此法中受檢標本不需稀釋,可直接用於測定,因此其敏感度相對高於間接法。乙肝標誌物中抗HBs的檢測常采用本法。本法關鍵在於酶標抗原的製備,應根據抗原結構的不同,尋找合適的標記方法。
(三) 間接法測抗體
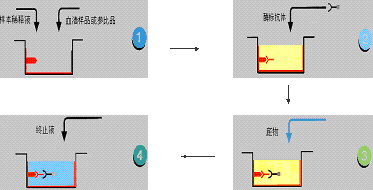
間接法是檢測抗體常用的方法。其原理為利用酶標記的抗抗體(抗人免疫球蛋白抗體)以檢測與固相抗原結合的受檢抗體,故稱為間接法(見圖2-3)。操作步驟如下:
(1)將特異性抗原與固相載體聯結,形成固相抗原。洗滌除去未結合的抗原及雜質。
(2)加稀釋的受檢血清,保溫反應。血清中的特異抗體與固相抗原結合,形成固相抗原抗體複合物。經洗滌後,固相載體上隻留下特異性抗體,血清中的其他成份在洗滌過程中被洗去。
(3)加酶標抗抗體。可用酶標抗人Ig以檢測總抗體,但一般多用酶標抗人IgG檢測IgG抗體。固相免疫複合物中的抗體與酶標抗體抗體結合,從而間接地標記上酶。洗滌後,固相載體上的酶量與標本中受檢抗體的量正相關。
(4)加底物顯色
本法主要用於對病原體抗體的檢測而進行傳染病的診斷。間接法的優點是隻要變換包被抗原就可利用同一酶標抗抗體建立檢測相應抗體的方法。
間接法成功的關鍵在於抗原的純度。雖然有時用粗提抗原包被也能取得實際有效的結果,但應盡可能予以純化,以提高試驗的特異性。特別應注意除去能與一般健康人血清發生反應的雜質,例如以E.Coli為工程酶的重組抗原,如其中含有E.Coli成份,很可能與受過E.Coli感染者血清中的抗E.Coli抗體發生反應。抗原中也不能含有與酶標抗人Ig反應的物質,例如來自人血漿或人體組織的抗原,如不將其中的Ig去除,試驗中也發生假陽性反應。另外如抗原中含有無關蛋白,也會因竟爭吸附而影響包被效果。
間接法中另一種幹擾因素為正常血清中所含的高濃度的非特異性抗體。病人血清中受檢的特異性IgG隻占總IgG中的一小部分。IgG的吸附性很強,非特異IgG可直接吸附到固相載體上,有時也可吸附到包被抗原的表麵。因此在間接法中,抗原包被後一般用無關蛋白質(例如牛血清蛋白)再包被一次,以封閉(blocking)固相上的空餘間隙。另外,在檢測過程中標本須先行稀釋(1:40~1:200),以避免過高的陰性本底影響結果的判斷。
(四)競爭法測抗體
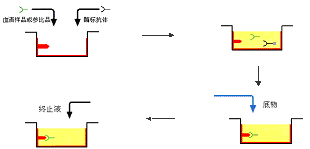
當抗原材料中的幹擾物質不易除去,或不易得到足夠的純化抗原時,可用此法檢測特異性抗體。其原理為標本中的抗體和一定量的酶標抗體競爭與固相抗原結合。標本中抗體量越多,結合在固相上的酶標抗體愈少,因此陽性反應呈色淺於陰性反應。如抗原為高純度的,可直接包被固相。如抗原中會有幹擾物質,直接包被不易成功,可采用捕獲包被法,即先包被與固相抗原相應的抗體,然後加入抗原,形成固相抗原。洗滌除去抗原中的雜質,然後再加標本和酶標抗體進行競爭結合反應。競爭法測抗體有多種模式,可將標本和酶標抗體與固相抗原競爭結合,抗HBc ELISA一般采用此法。另一種模式為將標本與抗原一起加入到固相抗體中進行競爭結合,洗滌後再加入酶標抗體,與結合在固相上的抗原反應。抗HBe的檢測一般采用此法。
(五)競爭法測抗原
小分子抗原或半抗原因缺乏可作夾心法的兩個以上的位點,因此不能用雙抗體夾心法進行測定,可以采用競爭法模式。其原理是標本中的抗原和一定量的酶標抗原競爭與固相抗體結合。標本中抗原量含量愈多,結合在固相上的酶標抗原愈少,最後的顯色也愈淺。小分子激素、藥物等ELISA測定多用此法。
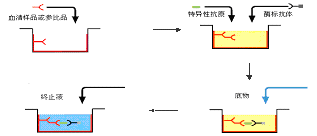
(六)捕獲包被法測抗體(經典方法)
IgM抗體的檢測用於傳染病的早期診斷中。間接法ELISA一般僅適用於檢測總抗體或IgG抗體。如用抗原包被的間接法直接測定IgM抗體,因標本中一般同時存在較高濃度的IgG抗體,後者將競爭結合固相抗原而使一部份IgM抗體不能結合到固相上。因此如用抗人IgM作為二抗,間接測定IgM抗體,必須先將標本用A蛋白或抗IgG抗體處理,以除去IgG的幹擾。在臨床檢驗中測定抗體IgM時多采用捕獲包被法。先用抗人IgM抗體包被固相,以捕獲血清標本中的IgM(其中包括針對抗原的特異性IgM抗體和非特異性的IgM)。然後加入抗原,此抗原僅與特異性IgM相結合。繼而加酶標記針對抗原的特異性抗體。再與底物作用,呈色即與標本中的IgM成正相關。此法常用於病毒性感染的早期診斷。甲型肝炎病毒(HAV)抗體的檢測模式見圖2-7.
類風濕因子(RF)同樣能幹擾捕獲包被法測定IgM抗體,導致假陽性反應。因此中和IgG的間接法近來頗受青睞,用這類試劑檢測抗CMV IgGM和抗弓形蟲IgM抗體已獲成功。
(七)ABS-ELISA法
ABS為親和素(avidin)生物素(biotin)係統(system)的略語。親和素是一種糖蛋白,分子量60000,每個分子由4個能和生物素結合的亞基組成。生物素為小分子化合物,分子量244.用化學方法製成的衍生物素-羥基琥珀酰亞胺酯可與蛋白質和糖等多種類型的大小分子形成生物素標記產物,標記方法頗為簡便。生物素與親和素的結合具有很強的特異性,其親和力較抗原抗體反應大得多,兩者一經結合就極為穩定。由於一個親和素可與4個生物素分子結合,因此如把ABS與ELISA法可分為酶標記親和素-生物素(LAB)法和橋聯親和素-生物素(ABC)法兩種類型。兩者均以生物素標記的抗體(或抗原)代替原ELISA係統中的酶標抗體(抗原)。在LAB中,固相生物素先與不標記的親和素反應,然後再加酶標記的生物素以進一步提高敏感度。在早期,親和素從蛋清中提取,這種卵親和素為堿性糖蛋白,與聚苯乙烯載體的吸附性很強,用於ELISA中可使本底增高。從鏈黴菌中提取的鏈黴親和素則無此缺點,在ELISA應用中有替代前者的趨勢。由於ABS-ELISA較普通ELISA多用了兩種試劑,增加了操作步驟,在臨床檢驗中ABS-ELISA應用不多。
科研項目中檢測微量的成分如細胞因子常采用本法。















 相關新聞
相關新聞