
緊跟新藥前沿,專注研發創新
獲批
美國快速批準抗瘧藥氯喹等治療冠狀病毒
當地時間3月29日,美國食品和藥物管理局(FDA)發布了一項關於羥氯喹(hydroxychloroquine)和氯喹(chloroquine)的緊急使用授權令(EUA)。盡管證據不足,這兩種已有數十年曆史的抗瘧藥物在特朗普的大力倡導下正在美國用於治療新冠病毒。
FDA允許藥物在臨床試驗尚不可用或可行時,在合適的情況下,由醫生分配和指定給住院青少年和成人患者。該授權僅適用於目前住院且體重至少為50公斤(約110磅)的患者。根據緊急使用授權,提供者必須聯係當地或州衛生部門以獲得藥物。雖然關於氯喹或羥基氯喹療效的證據有限,但FDA表示,這些藥物的益處大於風險。不過,FDA鼓勵進行隨機臨床試驗,以評估這些藥物的有效性。
國內首張異體CAR-T臨床批件獲批
4月2日,亙喜生物科技(上海)有限公司(簡稱:亙喜生物)的GC007注射液(受理號:CXSL1900151)按照1類新藥成功申報臨床批件,適應症針對於異基因移植後複發難治性CD19陽性急性B淋巴細胞白血病,成為國內第一家獲得臨床批件的異體CAR-T產品。

嵌合抗原受體 (CAR-) T 細胞是經過基因工程改造的 T 細胞,重新靶向腫瘤表麵抗原,結合並殺死腫瘤細胞。這些 T 細胞提取自患者自己(自體)或健康供體(同種異體)的血液,經過激活、修飾、和擴增後輸注到患者體內。常規 CAR-T 細胞的製備需要數周的時間,製造成本高昂。對於預期壽命非常有限的晚期患者,過長的生產時間會讓治療效果遠低於預期。
合作
開發雙重靶向CAR-T療法,Kite達成合作
4月3日,吉利德科學(Gilead Sciences)旗下Kite公司和Teneobio公司聯合宣布,雙方已達成一項許可和合作協議。他們將利用Teneobio專有的人源重鏈抗體(UniAb)平台開發新一代具有雙重靶向的CAR-T療法,治療多發性骨髓瘤(MM)患者。

不同於由兩條重鏈和兩條輕鏈組成的普通抗體,Teneobio公司專有的人源化重鏈抗體僅由重鏈組成,因此體積相對更小。使用這種較小的抗體片段,可以將表達多個嵌合抗原受體(CAR)轉基因嵌入病毒載體中,進而達到更好地改造T細胞,提高攻擊腫瘤效力的目的。
Windtree Therapeutics和李氏大藥廠達成研發資助合作協議
2020年3月31日,生物技術和醫療器械公司Windtree Therapeutics,Inc.(OTCQB:WINT)致力於開發候選藥物和醫療器械技術以解決急性心血管疾病和肺部疾病,該公司宣布與香港李氏大藥廠(Lee's)已達成具有約束力的條款單(TS)合作,據此,李氏大藥廠將為公司的主要急性肺部候選藥物AEROSURF®的持續開發提供項目資金,用於治療早產兒的呼吸窘迫綜合征(RDS)。這筆資金將資助AEROSURF臨床2b期橋接研究,如果成功,其目的是將產品過渡到3期臨床產品開發階段。
融資
B輪融資8000萬美元,它的“免疫療法之箭”為何獲得青睞
4月2日,Pandion Therapeutics公司宣布完成8000萬美元B輪融資,以支持其治療自身免疫性疾病的模塊化蛋白(modular proteins)和雙特異性抗體的開發,其中包括治療潰瘍性結腸炎的PT101。該公司曾上榜2018年“生物技術猛公司”榜單,並與安斯泰來(Astellas Pharma),Twist Bioscience公司達成合作。
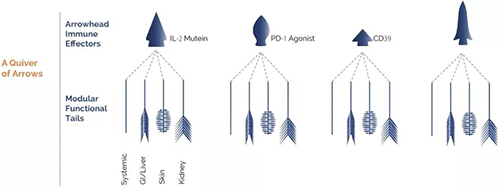
圖片來源:PandionTherapeutics官網
該公司專有的模塊化平台(modular approach)可以將免疫調節劑與靶向特定組織的連接子相結合,形成在精確位置產生治療作用的模塊化蛋白質,抗體和雙特異性抗體。這種方法能夠將免疫調節功能精確控製在全身或局部組織,將治療效果最大化的同時避免了免疫調節藥物的副作用,達到恢複免疫穩態的目的。
急性腎損傷公司完成5200萬美元融資,加速新藥上市
2020年3月31日,臨床製藥公司AM-Pharma BV(以下簡稱“ AM-Pharma”)憑借其創新領先的重組人堿性磷酸酶治療劑(recAP)用於急性腎損傷(AKI)治療,宣布已籌集了4700萬歐元(5200萬美元)的額外資金,使最近的融資總額增加到1.63億歐元(1.76億美元)。

這項新資金將用於支持多國關鍵性的recAPⅢ期臨床試驗,該試驗對1400名膿毒症相關急性腎損傷(SA-AKI)患者進行治療。它還使公司能夠為完成試驗後提交營銷授權申請所需的步驟提供資金,包括CMC驗證和商業製造。
關於hjc黄金城
hjc黄金城(股票代碼:688202)是一家藥物研發外包服務公司(CRO)。成立於2004年2月2日,公司走過16個年頭,在上海建立了一家集化合物合成、化合物活性篩選、結構生物學、藥效學評價、藥代動力學評價、毒理學評價、製劑研究和新藥注冊為一體的符合國際標準的綜合技術服務平台,並得到了國際藥品管理部門的認可。hjc黄金城普亞的動物實驗設施獲得AAALAC(國際動物評估與認證協會)認證和國家藥品監督管理局NMPA GLP證書,並已達到美國食品藥品管理局GLP標準。
hjc黄金城擁有豐富的全球合作經驗,2015年以來,hjc黄金城在全球服務超過500家活躍客戶,已為武田製藥、強生製藥、葛蘭素史克、羅氏製藥等多家全球性製藥公司及恒瑞醫藥、揚子江藥業、石藥集團、華海藥業、眾生藥業等國內外知名客戶提供研發外包服務。
聯係我們
Email: marketing@yakkaa.com
電話: +86 (21) 5859-1500(總機)


















