製藥行業對罕見病日益增長的興趣似乎沒有減弱的跡象,而這也有著充分的理由。日前,EvaluatePharma公司發表的一份最新孤兒藥研究報告發現,近年來,製藥行業對罕見病的研發投入不斷增加,由此形成的局麵是,孤兒藥在全球藥品銷售總額中所占據的份額不斷提高。
推動這種變化的主要因素有,孤兒藥麵臨的監管環境不斷向好,市場獨家銷售權和定價優勢使得這類藥物要比非孤兒藥更加有利可圖。值得注意的是,前25大非腫瘤領域的孤兒藥在未來6年裏的複合增長率預計將達到18%,這幾乎是市場平均水平的3倍。
暢銷孤兒藥排名變化
Esbriet、NovoSeven或將落榜,Spinraza、Exondys 51新進榜單
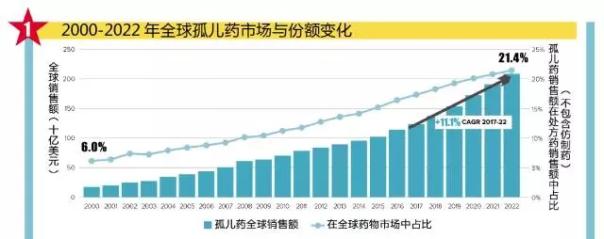
EvaluatePharma報告指出,2016年孤兒藥合計創造了1140億美元的銷售額,占全球非仿製藥市場的16.4%。到2022年,這一數值將上升至2090億美元,在整個藥品市場的占比達到21.4%。也就是說,在短短的10年時間裏,孤兒藥在藥品市場的份額將翻一番。
如果這些銷售預測如期實現,那麽,孤兒藥在未來6年裏的複合年均增長率將達到11.1%,大約是非孤兒藥的兩倍。
EvaluatePharma編輯和報告撰寫人厄克特(Lisa Urquhart)表示,小型生物技術公司在罕見病治療領域的實力不容小覷,但在今年的報告中,大型藥企在這一領域重新占據了主導地位。
這份報告采用的孤兒藥的定義是,首先被批準用於一種罕見病的藥物,或者被批準一種以上的適應症的藥物,但該藥在孤兒適應症的用途上所占的銷售額超過25%。
從狹義角度來看(不包括腫瘤學領域,隻涉及長期用來治療罕見、危及生命的疾病的那些藥物),到2022年,前25大孤兒藥將合計創造銷售額374億美元,在全球藥品的銷售額中占比約為3.8%。
當然,這一數據並沒有包括那些有著多種獲批治療用途的重磅炸彈級藥物,因為其大多數用途並不是針對罕見病。從更加狹窄的範圍來仔細考量孤兒藥是應該的,因為這可以較好地弄清楚這些高價孤兒藥在用於治療囊腫性纖維化和罕見溶酶體疾病等疾病上的總體費用。
到目前為止,在這些治療領域裏,孤兒藥麵臨的定價壓力很小,或者根本就沒有,它們在全球藥品銷售總額中至少占據個位數的百分比。不過,值得注意的是,這個市場有時會麵臨藥品支付方的阻力,原因可能在於,它們要在一小部分患者身上花費掉不菲的預算。
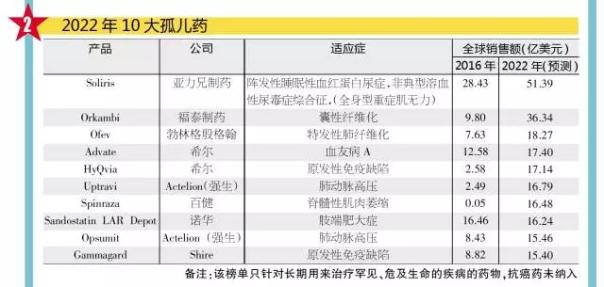
亞力兄製藥(Alexion)開發的超級孤兒藥Soliris仍然是這一領域的主打產品。Soliris的銷售額達到37億美元,在所有製藥產品銷售榜上排名第27位。隨著該藥預計被批準用來治療全身型重症肌無力,到2022年,Soliris的銷售額預計將上升到51億美元。據此,EvaluatePharma預測,Soliris將成為製藥行業第9大暢銷藥物。
將EvaluatePharma 2015年的孤兒藥報告進行比較之後,可以發現,頂級孤兒藥之間的排名也出現驚人的變化。比如,根據此前市場普遍達成的預測數據,到2020年,羅氏(Roche)和諾和諾德(Novo Nordisk)的藥物Esbriet和NovoSeven都將處於前列,但是現在,它們有可能在2022年的排行榜上消失,可能是因為它們針對的適應症發生了競爭性的變化。
近幾個月來,在孤兒藥領域,百健(Biogen)和Sarepta公司相繼推出了用來治療脊髓性肌萎縮的藥物Spinraza和用來治療杜氏肌營養不良(DMD)的藥物Exondys 51。前者預計將在2020年進入前10大孤兒藥行列,而後者會進入前30大孤兒藥行列。不過,從目前的情況來看,在美國,藥品支付方均對這兩隻藥物采取了限製使用的措施。
新基醫藥領銜孤兒藥市場
BMS、諾華、羅氏與強生緊隨其後
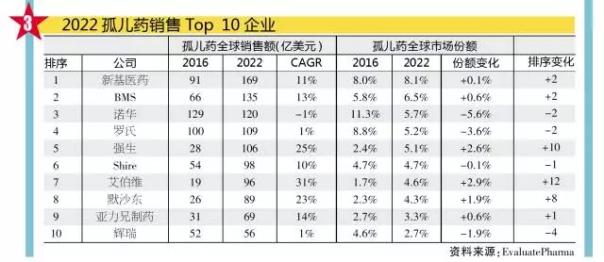
報告指出,到2022年,新基醫藥(Celgene)預計將在孤兒藥的銷售上超越所有競爭對手,這要歸功於其所銷售的血癌藥物來那度胺(Revlimid)。該藥的銷售額預計將從2016年的近70億美元增加到2022年的135億多美元。早在2005年,該藥就已獲批用於孤兒適應症,被用來治療骨髓增生異常綜合征。自那時起,它又相繼被批準用於治療非霍奇金淋巴瘤和多發性骨髓瘤等孤兒適應症。
此外,百時美施貴寶(Bristol-Myers Squibb)、諾華(Novartis)、羅氏(Roche)和強生(Johnson & Johnson)將在這份排序名單上緊隨新基醫藥之後。EvaluatePharma在報告中預測,百時美施貴寶的檢查點抑製劑藥物Opdivo將成為2022年歐洲市場上最暢銷的孤兒藥。
去年,孤兒藥讓每位患者平均支付了140443美元,而非孤兒藥的數據為27576美元。通過采用中位數價格,EvaluatePharma分析師發現,2016年,每位患者在孤兒藥上的費用支出要比非孤兒藥高出5.5倍。
雖然有著嚴格的定義,但孤兒藥仍然是藥品開發最火爆的領域之一。從公共政策方麵來考量,針對它們的法律框架被普遍認為取得了巨大的成功。然而,今後的風險在於,孤兒藥可能在不久之後將麵臨著非孤兒藥常見的、相同的定價壓力。
這份研究報告的發表,正值美國參議員查爾斯·格拉斯利(Charles Grassley)承諾要對美國孤兒藥法律展開研究之際。《孤兒藥法案》於1983年頒布,為那些願意參與罕見病治療的製藥公司提供了開發動力和獨家保護權,但格拉斯利表示,對這項法律的“非預期使用”可能讓納稅人付出了較大的代價。














 相關新聞
相關新聞