
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




科研人員在篩選藥物活性的時候,往往希望得到活性較高的化合物,不過,通過多年的研究發現,藥物對靶點的選擇性高,活性強,未必會是一劑良藥,甚至不能成藥,為了得到較好的療效和較低的不良反應,化合物的成藥過程需要權衡各方麵的利弊。而針對全新靶點設計並成功上市的首創型藥物,往往也很難即刻得到醫生和患者的認可,以及市場長時間的考驗!因此,如何將已知靶點進行更為深入、更為全麵的研究,並通過大量的數據而設計出療效更好的藥物,就顯得尤為重要。從近年來上市的藥物來看,多靶點藥物得到了更為廣泛的關注和青睞,那麽,多靶點藥物有哪些優勢?如何設計多靶點藥物?多靶點的藥物設計,容易嗎?它是否會成為今後藥物研發的一大主流呢?今天,我們就聊聊多靶點藥物的那些事!
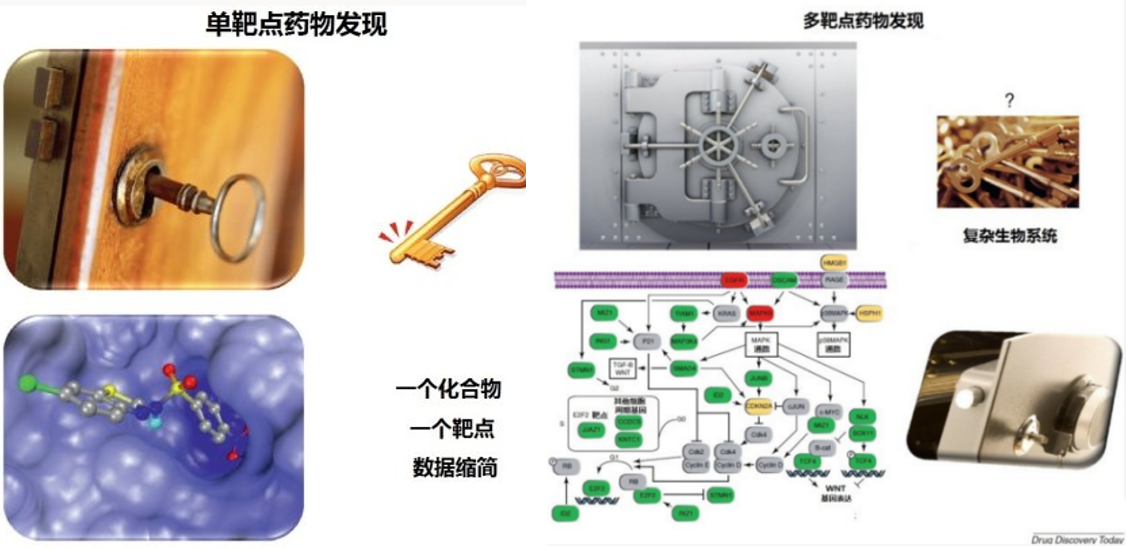
自從上個世紀,科學家提出鎖匙模型以後,藥物的發現逐漸集中於開發單靶點藥物,即努力將配體和特異性靶點完美的結合起來,該模型直至今天,仍在廣為流傳。不過,經過多年的探索,這種點對點的“打擊”似乎並不十分奏效,畢竟人體是一個有機整體。因而,多靶點藥物的概念逐漸增強,並通過多年的發展,已有多個藥物上市,對疾病的治療得到了進一步的補強!
所謂多靶點藥物,是指同時作用於疾病網絡中多個靶點的藥物,對各靶點的作用產生協同效應,使總效應大於各單效應之和,達到最佳的治療效果。目前已上市的、較為突出的多靶點藥物主要集中在抗腫瘤、心血管、神經係統等方麵,如抗腫瘤藥物的索拉非尼、達沙替尼、舒尼替尼、拉帕替尼;心血管藥物奧馬曲拉、特波格雷、普齊地洛;中樞神經係統藥物拉多替吉、奧氮平、卡巴拉汀等等。
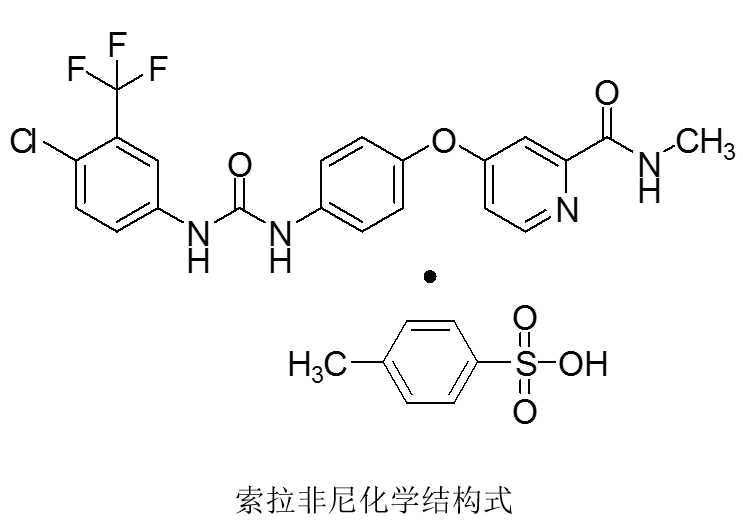
索拉非尼(Sorafenib),商品名“多吉美”,是拜耳和ONYX公司共同研製的一種小分子多靶點口服抗癌藥物,不僅能抑製VEGFR、PDGFR、FLT3和KIT受體酪氨酸激酶活性,而且還是Raf激酶的強效抑製劑。早在2005年12月,美國FDA就批準其用於治療晚期腎癌,後2007年11月,美國FDA再次批準其用於無法切除治療的晚期肝癌。該藥在我國分別於2006年和2008年被批準用於晚期腎癌和晚期肝癌的治療。2011~2015連續五年,索拉非尼的年銷售額超過10億美元。
最初,索拉非尼是在對c-Raf激酶的抑製劑先導物進行結構-活性評價的生化分析中被發現的。通過對20萬個化合物進行高通量篩選,發現了活性微弱的3-噻吩基脲,為了提高活性,利用組合化學的平行合成技術,設計了一個約1000個雙芳基脲的小分子化合物庫來研究3-噻吩基脲的構效關係,從而改善對Raf-1激酶的抑製活性,篩出了一個活性相對較好的3-氨基異惡唑脲化合物,繼續結構優化,最終發現了索拉非尼的結構。
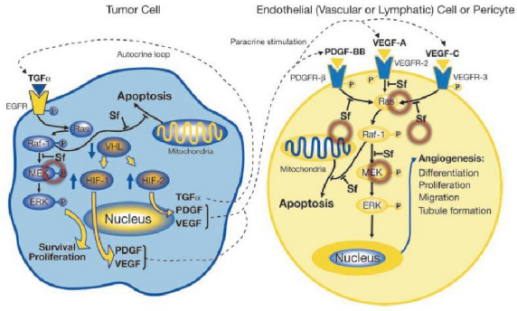
索拉非尼通過抑製c-Raf和b-Raf的絲氨酸/蘇氨酸激酶活性,進而抑製Raf-MEK-ERK信號傳導通路,最終抑製腫瘤細胞的生長。其對Raf激酶的多種亞型都存在抑製作用,作用強度依次為c-Raf>野生型b-Raf>突變型b-Raf。研究表明,索拉非尼對c-Raf的IC50值為6nmol·L-1,對野生型b-Raf的IC50值為25nmol·L-1,對突變型b-Raf的IC50值為38nmol·L-1。進一步研究發現,索拉非尼還能抑製人VEGFR-2、VEGFR-3、PDGFR-β、FLT3和c-KIT的酪氨酸激酶活性。索拉非尼激酶活性抑製試驗表明,其抑製VEGFR-1,VEGFR-2和鼠VEGFR-3的IC50分別為26,90和20nmol·L-1。
總的來說,索拉非尼一方麵通過抑製c-Raf激酶及下遊信號傳導、阻礙MEK和ERK的磷酸化過程、降低ERK的磷酸化水平,發揮抗細胞增殖的作用。另一方麵索拉非尼通過抑製VEGFR-2、VEGFR-3和PDGFR-β,抑製酪氨酸激酶受體的自身磷酸化過程,而發揮抗血管生成的作用。同時還可以抑製啟始因子-4E的磷酸化過程、下調體內抗凋亡蛋白Mcl-1的水平,發揮促細胞凋亡作用等等。
索拉非尼的“一石二鳥”、“雙管齊下”,讓人們在抗腫瘤的長征路上邁進了一步,看到了多靶點藥物的優勢。多靶點藥物的優勢,與單靶點藥物相比,主要存在以下三方麵的優勢。
首先,在研究模式方麵,單靶點藥物存在著“本質”上的缺陷。由於單靶點藥物隻能調控疾病發生過程中的一個環節,而各種臨床重大疾病包括惡性腫瘤、心腦血管疾病、神經退行性疾病和代謝性疾病等通常是多因素共同作用的結果,具有多種發病機製、多個病理環節和多基因相關性等,其病因病理機製及疾病進展過程非常複雜,單靶點藥物隻能抑製一種細胞信號分子,因此往往會導致治療效果不佳,同時也造成藥物篩選效率不高。而多靶點藥物可以同時作用於同一疾病的多個病理環節、多種發病機製而產生協同作用效果,使總效應大於單效應之和,從而提高藥物的療效。
其次,在毒副作用方麵,也是限製單靶點藥物臨床廣泛應用的一個重要原因。藥物靶標通常處於多個信號通路中具有多重生物學功能,過分激活或抑製體內某一生物靶標分子,在幹預其一種生物學功能的同時,也可以影響其它正常生物學功能以及與其相關的其它生物大分子的正常功能,從而導致毒副作用的發作。多靶點藥物可以更好的平衡同一疾病的多個病理因素間的關係,可以在相對更低的血藥濃度水平,協同作用產生單靶點藥物需要高濃度才能產生的生物學效應,且對生物靶標一般具有弱親和力的特點,因此不會強烈抑製或激活某一藥物靶點,因而可以減少藥物的不良反應。
再次,生物機體是一個複雜的可自我調節和平衡的網絡係統,長期使用某一單靶點藥物治療疾病,可以誘導機體內部的適應性變化而激活對抗保護機製或者旁路代償機製等,使疾病對該種藥物不再敏感,造成藥物的耐藥性,如單藥治療晚期腫痛患者經常會造成多藥耐藥和治療失敗等。而多靶點藥物可以通過同時幹預同一疾病的主要致病靶標及其代償信號通路或者其保護性信號通路而減少疾病對藥物產生的耐藥性。
多靶點藥物分子的合理設計方法主要是組合藥效團法,其又可分為偶聯藥效團法、融合藥效團法和合並藥效團法。偶聯藥效團法是設計多靶點藥物的最重要方法之一,又分為可分解性和不可分解性。其優點是適用範圍廣,幾乎所有單靶點配體分子都可以通過這種方法連接成多靶點藥物。另外,該類多靶點藥物可以同時針對疾病相關的所有信號通路的靶標進行組合設計,全麵調節疾病的各個病理環節而實現最佳的治療效果、最小的毒副作用和最低的耐藥現象。該法的缺點是設計的多靶點藥物分子通常相對分子量較大(常大於500)溶解度和口服吸收較差等。偶聯藥效團法設計多靶點藥物實際上早就已經應用於藥物開發,如經典抗菌藥物舒他西林就是采用亞甲基為連接子將半合成抗生素氨苄西林與β-內酰胺酶抑製劑舒巴坦連接形成的多靶點抗菌藥物。
合並藥效團法是設計多靶點藥物的另一個重要方法,該法是基於同一疾病相關的不同靶點的配體或配體結合位點的結構相似性而實現的,同一疾病相關的不同藥物靶點可能屬於同一類型不同亞型的受體、酶或離子通道等,其配體結合位點常存在相似性如空問結構、電性或者疏水性等方麵相似,能夠兼容結合結構類似的小分子配體,可以根據這種相似性而采用合並藥效團法設計多靶點藥物,尤其可利用計算機輔助藥物設計技術(CADD)進行基於受體相似性的多靶點藥物合理設計,而顯著提高藥物設計的效率。合並藥效團法的優點是可以獲得相對分子量較小、理化性質較適宜和藥代動力學特性較好的多靶點藥物,其成藥幾率較高,缺點是適用範圍較小,隻適用於不同靶點的配體或配體結合位點結構相似的情況,而當這種相似性存在時,則這些不同靶點的功能也通常具有相似性,因而就難以更全麵的調節複雜疾病的不同病理環節,顯然難以獲得最佳療效。
多靶點藥物設計的困難在於其限製因素較多,需要協調平衡多方麵參數使之處於適度區間。如藥效學方麵需要考慮靶標組合的合理性、活性的平衡性和靶標的選擇性;藥動學方麵,要考慮ADME各方麵特性的適當與否;在化學方麵,要考慮其理化性質的合適與否等;靶標組合方麵,它要求選擇疾病病理機製中最關鍵的幾個靶標進行組合,並且不同靶標間應該具有協同作用效果,即總效應大於各靶標分效應之和,這樣才能保證靶標組合的合理性;活性平衡方麵,它要求多靶點藥物對各靶點的作用強度接近而不宜差別太大,盡量使它們的EC50或IC50值接近;靶標選擇方麵,要求多靶點藥物隻選擇作用於所確定的靶標組合,而不應對其他靶標有多餘的活性,以減小不必要的副作用。
由於多靶點藥物各參數間的相互影響,一般需要在其各種性質之間作必要的妥協和平衡,另外多靶點藥物研究中選擇高質量的配體先導物也是提高其設計成功率的一個方麵。盡管存在很多問題和困難,多靶點藥物的高療效和低毒性等優勢己引起人們的廣泛關注,隨著現代係統生物學、化學生物學以及計算機輔助藥物設計技術等的發展,多靶點藥物研究必將取得更大的進步。
當下,創新藥物的研發是“形勢所迫”,同時也是“大勢所趨”。形勢所迫,迫於仿製藥的一致性評價,大勢所趨,趨於人類的不斷進步。我國目前對於創新藥物的研發能力,大多處於me-too,最好也就是me-better。對靶點的研究水平還無法和大型跨國製藥公司相提並論,就更別提對全新靶點的探索了。那麽,對已知靶點合理的、最大可能的利用就顯得格外重要,多靶點藥物的合理設計,也許能為我們帶來更多、更好、更有競爭力的產品。即便短期不能為我們的藥物研發帶來明顯的收益,但這種思路還是值得擁有的!
參考文獻:
1. Zimmermann GR,Lehar J, Keith CT. Multi-target therapeutics: when the whole is greater thanthe sum of the parts[J]. Drzag Discov Toclcry, 2007, 12(1-2): 34-42.
2. Hopkins AL.Network pharmacology: the next paradigm in drug discovery[J]. Ncrt Chem Biol,2008, 4(11): 682-690.
3. Sorbera LA,Castaner J, Fresno M, et al. Netoglitazone[J]. Drugs F'ut, 2002, 27(2): 132-13.
4. 邊海勇.新型多靶點抗腫瘤維甲酸類衍生物的設計,合成與生物活性研究[D].2011.
5. 錢文麒,韓偉,唐三植等。多靶點藥物的開發策略及研究進展[J].廣東化工,2014,8(41):69.
6. 郭彥伸,郭宗儒。多靶點藥物分子設計[J].藥學學報,2009,44 (3): 276−281.
 相關新聞
相關新聞