
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




泛素-蛋白酶體係統(UPS)功能紊亂與多種疾病的發生具有密切關係,包括腫瘤、心血管疾病、神經退行性疾病等。因此,UPS已經成為相關疾病治療的熱門靶點之一。抑製泛素-蛋白酶體係統,調控相關底物蛋白的降解,實現疾病治療是重要的藥物開發策略,目前靶向泛素-蛋白酶體係統的小分子抑製劑研究主要有泛素活化酶E1抑製劑、泛素結合酶E2抑製劑、泛素連接酶E3抑製劑以及蛋白酶體抑製劑等。
TAK-243是一種首創的(First-in-Class)、高效的泛素活化酶E1 (UAE) 抑製劑。研究發現TAK-243具有顯著的抗腫瘤活性。其中,科研人員通過hjc黄金城使用HCC-70模型進行體內藥效實驗。結果發現腫瘤生長抑製率(TGI)達到91%。本篇文章結合文獻報道和hjc黄金城藥效部門的經驗,分享泛素化抑製劑研發的藥效研究案例,希望對關注泛素化研究和腫瘤藥效的各位科研工作者有所幫助。
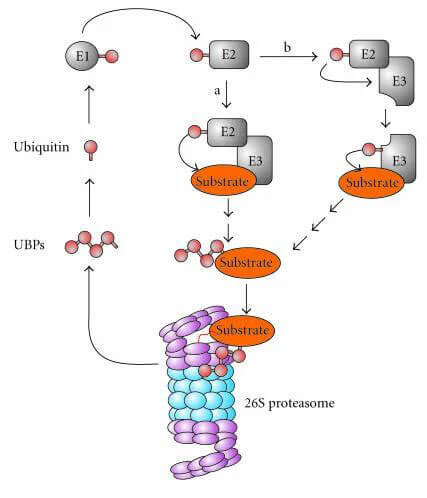
泛素-蛋白酶體係統(UPS)[1]
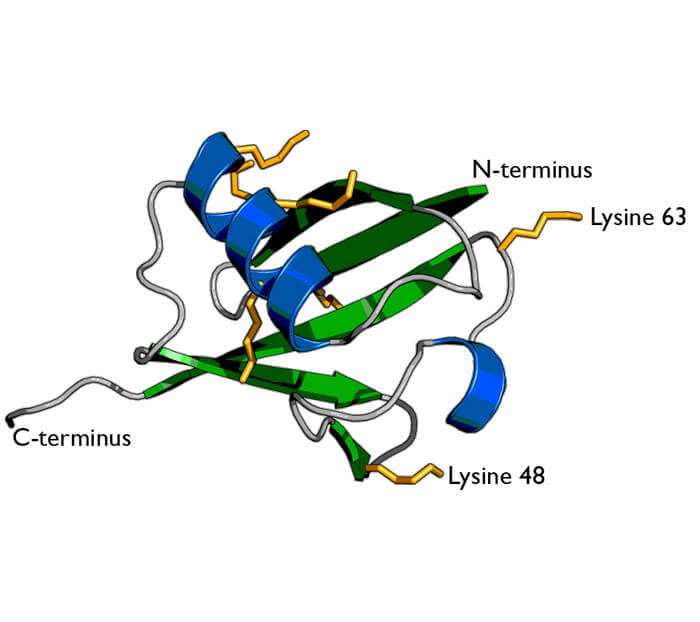
泛素結構圖(來源:Wikipedia)
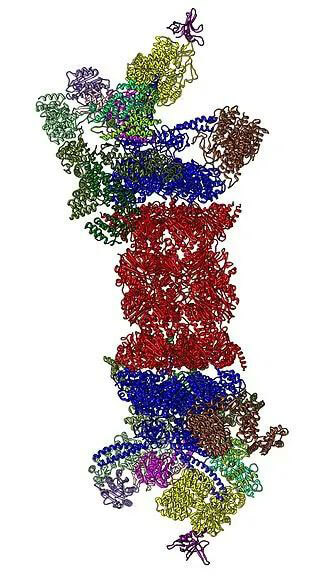
26S蛋白酶體結構(來源:Wikipedia)
❖ 在ATP供給能量的情況下,泛素活化酶E1將泛素分子活化;形成E1-泛素的中間產物;
❖ 泛素活化酶E1將活化的泛素分子傳遞給泛素結合酶E2;形成一個E2-泛素的中間產物;
❖ 泛素連接酶E3先識別待降解的靶蛋白,再將結合E2的泛素連接到靶蛋白上,形成一個包含E2-泛素中間產物、E3 酶和靶蛋白的複合物;
❖ E2 酶和E3 酶,從上述的複合物中釋放,從而形成被泛素標記的靶蛋白;
❖ 重複上述過程,直到蛋白質上連接的多個泛素形成一條泛素鏈;
❖ 被泛素化的靶蛋白,被26S 蛋白酶體識別和降解。
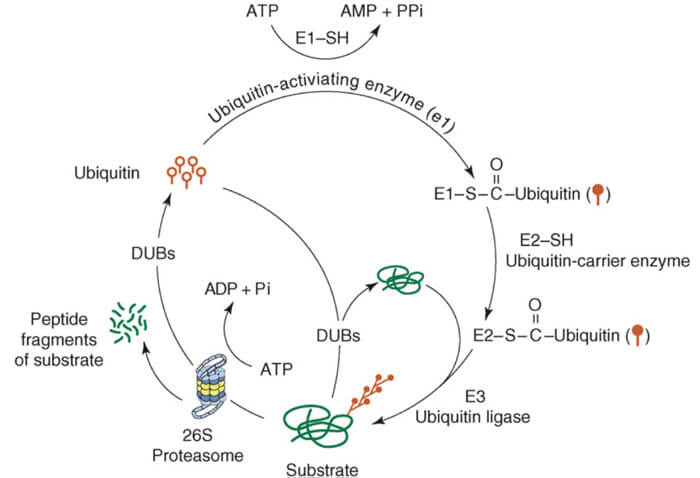
泛素-蛋白酶體途徑[2]
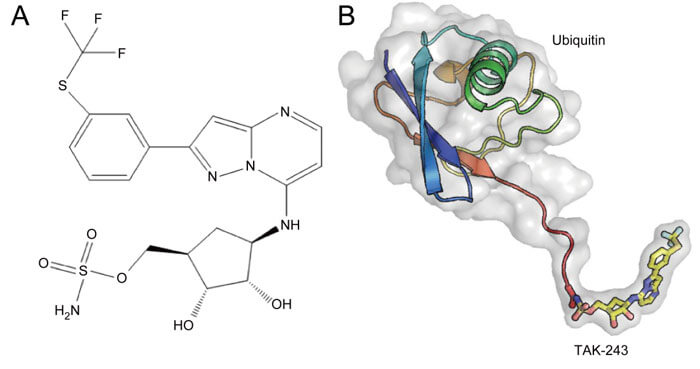
A: TAK-243 的化學結構 B: TAK-243-泛素加合物的結構[3]
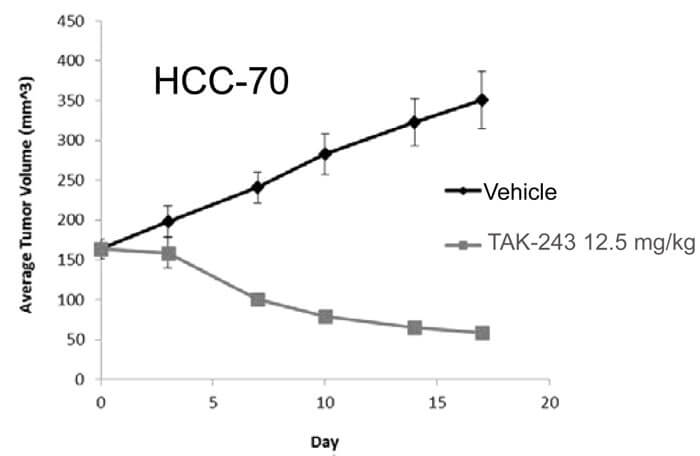
TAK-243對HCC-70的生長抑製曲線[3]
研究發現 TAK-243 在所有檢查的模型中都誘導了顯著的抗腫瘤活性反應。其中對CWR22、PHTX-235O、HCC-70和PHTX-55B的TGI達到90%以上。同時對動物體重幾乎沒有影響。
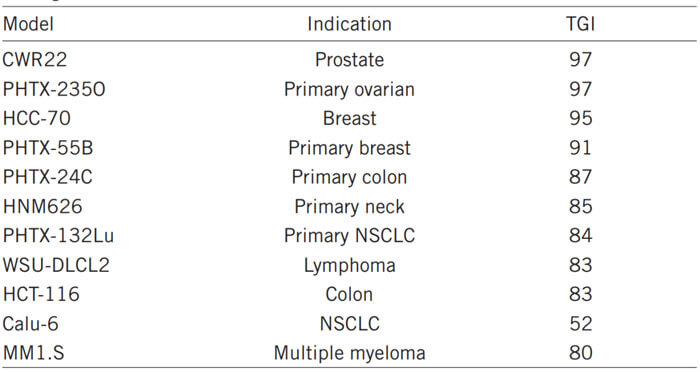
TAK-243體內抗不同腫瘤的活性[3]
[1] Marie W Wooten, et al. Signaling, polyubiquitination, trafficking, and inclusions: sequestosome 1/p62's role in neurodegenerative disease. J Biomed Biotechnol. 2006;2006(3):62079.doi: 10.1155/JBB/2006/62079.
[2]Ashok N Hegde, et al. The ubiquitin-proteasome pathway in health and disease of the nervous system. Trends Neurosci. 2007 Nov;30(11):587-95. doi: 10.1016/j.tins.2007.08.005. Epub 2007 Oct 24.
[3]Marc L Hyer, et al. A small-molecule inhibitor of the ubiquitin activating enzyme for cancer treatment. Nat Med. 2018 Feb;24(2):186-193. doi: 10.1038/nm.4474. Epub 2018 Jan 15.
[4] Isabella A Lambert-Smith, et al. The pivotal role of ubiquitin-activating enzyme E1 (UBA1) in neuronal health and neurodegeneration. Int J Biochem Cell Biol . 2020 Jun;123:105746. doi: 10.1016/j.biocel.2020.105746. Epub 2020 Apr 18.
[5] H. Yang, X. Chen, K. Li, et al. Repurposing old drugs as new inhibitors of the ubiquitin-proteasome pathway for cancer treatment. Seminars in Cancer Biology. 2021, 68:105-122.
[6] L. Cappadocia, C. D. Lima. Ubiquitin-like Protein Conjugation: Structures, Chemistry, and Mechanism. Chem Rev. 2018, 118(3): 889–918.
[7] J. A. Harrigan, X. Jacq, N. M. Martin, et al. Deubiquitylating enzymes and drug discovery: emerging opportunities. Nat Rev Drug Discov. 2018, 17(1): 57–78.
❖ 已建立將近300種腫瘤評價模型,同時我們為創新療法賦能,全麵布局腫瘤免疫療法的評價和研究,已完成CAR-T,TCR-T, CAR-NK, 溶瘤病毒, 抗體(單抗,雙抗,多抗等),siRNA, AAV等免疫療法的模型建立及藥效評價。
❖ 根據客戶的需求提供各種有效的動物模型(腎衰模型、貧血動物模型、胃酸分泌動物模型、胃潰瘍模型等),用來檢測藥物的有效性。常規的消化係統疾病有:胃酸分泌、胃潰瘍、腎衰等,通過大鼠進行動物實驗。
❖ 在代謝性疾病領域具有數十個穩定有效的動物模型,尤其對於臨床缺乏有效藥物治療、且近期研發火熱的NAFLD疾病領域具有豐富的經驗和有效的動物模型。
❖ 為炎症免疫疾病藥物的藥效評價提供了多種針對不同靶點及通路,穩定可靠,擁有良好評價能力的動物藥效評價模型,為新藥的臨床轉化提供助力。
❖ 建立了涵蓋抗抑鬱藥、抗老年癡呆症藥、鎮靜催眠抗焦慮藥、鎮痛藥、抗驚厥藥、抗帕金森氏症藥以及抗精神分裂症藥等眾多疾病精神係統疾病模型評價技術,可以從分子水平、細胞水平、Ex-vivo、invivo等多層麵全麵評價一類創新藥物。
❖ 根據客戶的需求提供各種有效的動物模型,常規的動物模型有:全層皮膚創傷疾病動物模型、壓瘡潰瘍疾病動物模型、自發性高血壓大鼠疾病動物模型等,通過大小鼠、SHR大鼠等進行動物實驗。
 相關新聞
相關新聞