30年後科學家找到敗血症研究新模型
2018-03-13
|
訪問量:{"id":1,"bid":"28.43","change":"-0.96","shishi":"27.47","jinkai":"28.15","change_rate":"-3.38","change_rate_html":"(-3.38%)","high":"28.73","low":"27.46","volumn":"2193321","turnover":"6119","turnover_num":0.61,"time":1721806620,"time_date":"PM 15:37\u20222024-07-24"}
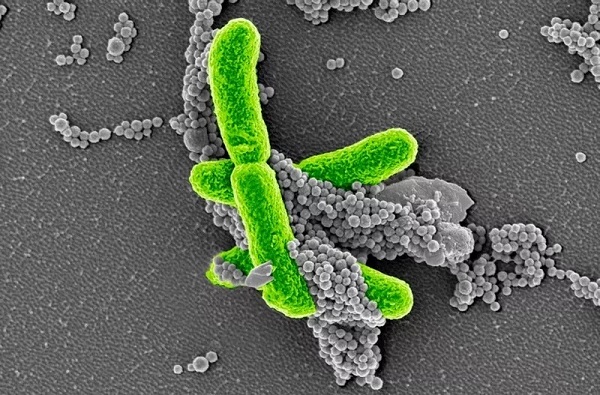
敗血症發生在身體響應自身組織和器官的感染性損傷之時,會導致器官的衰竭。
圖片來源:Wyss Institute at Harvard University
在全球範圍內,每年有上百萬人因敗血症而死亡,這也是已經入院治療後的患者常見的死亡原因。盡管敗血症的發病率很高,但是目前能夠提供給患者的標準治療方式是使用抗生素治療。自從30年前一次敗血症治療的臨床試驗以高失敗率而告終後,一直沒有新的治療方式被開發出來。
臨床前試驗中經常用來進行藥物評估的動物模型往往來自於小鼠或者狒狒,但是對於敗血症來說,它們並不是一個好的參考模型,因為,對於導致人類敗血症的感染,這些動物經常是能夠抗擊這些病原體的。豬成為了一個較為合適的選擇,因為它們80%的免疫係統與人類具有一樣的機製,凝血也很相似,並且由於它們較大的體型使得它們的生命體征很容易被監測。
雖然,有著這樣的較為充分的原因,但是在實際的操作中,還是麵臨著種種困難的。在對豬進行的研究中,往往由於沒有合適的設備、人員和臨床設施而受到限製。
為了攻克這一問題,來自哈佛大學威斯研究所的科研人員與波士頓兒童醫院合作,開創了一種新的臨床監測方法,用以監測豬對於敗血症的生理響應。分析這些豬在器官衰竭時的多重生理表征,能夠為臨床前敗血症藥物作用於人體提供精確的預測。研究發表在最近的《Advances in Critical Care Medicine》上。
人類的敗血症評估是基於2016年稱為敗血症-3(Sepsis-3)的指南,使用了順序性器官衰竭評估(SOFA)評分標準,通過結合對心髒、腎髒、肝髒、肺、大腦以及凝血功能的測量,基於嚴重程度對敗血症進行分類。敗血症會導致多器官的衰竭。一般來說,動物模型是根據動物是否因病死亡而進行評估的,確切的原因隻在屍檢中確定。受臨床上敗血症-3評估的啟發,研究人員開創了一種豬特異性敗血症-3(ss-Sepsis-3)的指南,以及豬特異性-SOFA(ss-SOFA)的評分標準,這樣研究人員就可以在活體的被感染的豬身上進行敗血症的評估,以人類臨床評估的方式進行。
“我們的係統超出了簡單的測量病原體感染對炎症以及動物存活率的影響。因為它模擬了在人類患者身上所能觀察到的危及生命的器官衰竭,它也可能對敗血症治療在人體上的表現提供一個很好的預測,”威斯研究所首席高級科學家聯合作者之一Mike Super博士談道。
本次研究的團隊,在其中他們向8隻年輕的約克夏豬體內注射了大腸杆菌(E.coli),依照指南評價他們對多種器官的實時響應。6隻豬在有意識的情況下被注射了細菌,而6隻在麻醉狀態下被注射了細菌,還有6隻沒有被注射大腸杆菌但接受了相同的程序(其中4隻有意識,2隻被麻醉)。科學家們在有意識和被麻醉的豬中都發現了總的ss-SOFA評分的增加,在很大一部分上是由於腎髒及凝血的衰竭,有兩個有意識的動物進一步發展為急性腎衰竭。
有3隻被麻醉的動物被定義為出現感染性休克(ss-SOFA係統中的最高嚴重程度),基於這些器官的衰竭綜合所致,敗血症引發了心髒衰竭,並且由於體溫下降而沒有引發發燒。這些結果表明,當對敗血症進行評估時,麻醉的影響需要被考量在內。
研究人員建立的這種新型的模型和評價體係,通過該係統可以對敗血症的嚴重程度進行量化,用於評價長期研究、不同類型病原體,以及抗生素治療和並發症情況。無論對有意識的或者是被麻醉的動物進行實時監測都需要大量的人員和時間投入,但是卻可以更接近的複製和研究人類敗血症的響應,對於這個疾病的藥物開發和測試來說是有著巨大意義的。
參考資料:
[1] A new model for an old killer

分享到:















 相關新聞
相關新聞