美國孤兒藥認定審評加速,我國孤兒藥研發順勢發展
孤兒藥是用於診斷、治療和預防罕見病的藥品。根據世界衛生組織(WHO)的定義:罕見病為患病人數占總人口數0.65‰~1‰的疾病,世界各國根據每個國家自己的情況,對罕見病的認定標準存在一定的差異,大多數是以患病率或患病人數作為罕見病的界定標準。
從20世紀80年代以來,孤兒藥的開發問題開始逐漸引起社會的關注,有很多國家和地區還成立了罕見病相關機構或組織,製定了專門的法律法規以促進孤兒藥的開發。隨著全球各國的日益重視,罕見病治療藥物的研究和開發逐漸成為大型製藥公司的重點。
2016年,全球孤兒藥的銷售額為1140億美元,比2015年增加12.2%。據EvaluatePharma預計,2022年全球處方藥市場可達1.06萬億美元,其中,32%的銷售額增長將來自孤兒藥產品,未來5年的年複合增長率將達到11%,比處方藥增長率(5.3%)的兩倍還多,孤兒藥的重要性已經彰顯。
美國:孤兒藥新藥占比重,
首次獲批適應症超六成
自1983年美國實施《孤兒藥法案》以來,孤兒藥在每年FDA批準的新藥中占有很大的比重。FDA對於孤兒藥的注冊采取“先孤兒藥認定,後上市審批”的方式。

自1983年以來,FDA已批準上市孤兒藥625項,獲得孤兒藥資格的近4200項,其中2017年上半年(截至6月30日),FDA批準孤兒藥37項(按適應症統計),授予孤兒藥資格256項。
近五年來,FDA批準的孤兒藥數量快速增長,2017年上半年已經超過2016年全年的獲批數量。
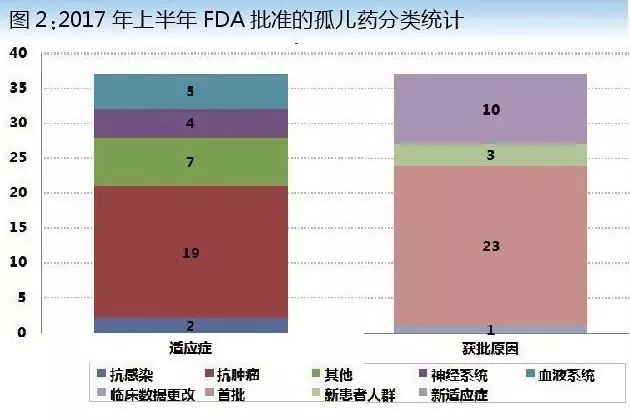
近年來,製藥產業界的研發熱點主要集中在抗腫瘤、抗感染、神經係統疾病以及血液係統疾病等方麵,而孤兒藥在各領域都有一席之位,其中抗腫瘤孤兒藥獲批19項,占獲批總數的50%以上。在已獲批的37個適應症中,23項為首次獲批,超過總數的60%,也體現了美國孤兒藥研發領域的絕對實力。

中國:漸接軌國際,
本土企業開始涉足研發,發展空間大
我國目前尚未有對罕見病的官方定義以及孤兒藥認定標準的明確界定,缺乏明確的政策法規和專門的審批部門。目前中國孤兒藥自主研製市場幾近空白,主要依賴進口。1983~2011年美國上市的360種孤兒藥中,僅有近60種在中國上市,品種多為2002年之前在美國以孤兒藥資格上市的抗艾滋病藥物、抗結核藥物、惡性瘧疾、麻風病、囊蟲病、隱球菌性腦膜炎、腸阿米巴病等藥品。另外,由於缺乏專門針對孤兒藥的遴選機製,報銷目錄中孤兒藥覆蓋率低,報銷比例不高,可及性低。
隨著社會對罕見病的重視,罕見病和孤兒藥逐漸進入我國政策法律的視野,一些激勵企業研發孤兒藥的政策陸續出台。2009年CFDA製定了《新藥注冊特殊審批管理規定》,明確規定對治療艾滋病、惡性腫瘤、罕見病等疾病且具有明顯臨床治療優勢的新藥實行特殊審批。國務院在“十二五”規劃中提出鼓勵罕見病用藥的研發,隨後CFDA出台一係列新藥審批改革政策對罕見病等特殊群體用藥給予單獨審評通道、多途徑動態補充資料以及審批時間縮短等特殊政策。
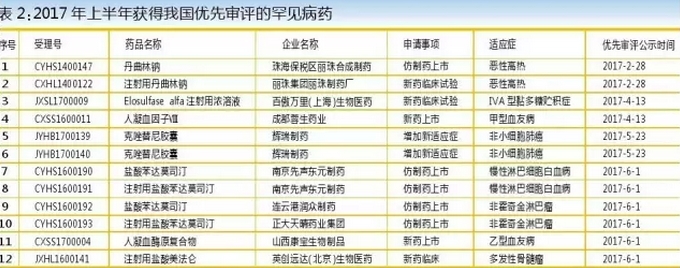
在國家激勵政策的支持下,本土企業也紛紛涉足孤兒藥的研發領域。根據CDE在2017年上半年發布的信息統計數據,有12項罕見病藥被列入優先審評。相比美國,我國孤兒藥研發仍有很大的距離。
美國孤兒藥研發熱潮高漲離不開美國優厚的激勵政策。美國、歐盟等國家設立了專門的孤兒藥認證和管理部門,並以《孤兒藥法案》為起點,陸續建立了完善的孤兒藥政策法律體係,包括:研發資助計劃;新藥申請費豁免、臨床試驗申報加速審批機製、加速審評、優先審評券、最高70%稅收優惠以及市場獨占權等政策,為罕見病用藥的發展注入了生機與活力。
相對而言,中國孤兒藥研發尚處於起步階段,但基於我國人口基數龐大,孤兒藥在我國的醫療需求將有巨大的空間。同時,我國正在麵臨著醫藥產業升級的關鍵時期,鼓勵企業開發可及性高的孤兒藥將具有重要的社會意義與經濟價值。據數據顯示,2016年中國胃癌、肝癌、食道癌的患者分別為679.1萬人、466.1萬人、477.9萬人,而這些疾病在美國被歸為罕見病。因此,在醫藥產業全球化戰略的熱潮下,開發這些孤兒藥或將成為中國藥企實現美國市場占領一席之地的快速通道。
結語<<<
政府幹預是保障罕見病患者權益的有效措施,在鼓勵我國孤兒藥研發、提高國家專科藥品可及性方麵,我國仍有很多可為之處。期待我國能夠借鑒美國等先行國家的經驗,製定符合中國具體國情的孤兒藥研發激勵政策,擴大孤兒藥的醫保範圍,提高可及性,燃燒本土企業的研發熱情,推動中國孤兒藥的發展,造福罕見病患者。

分享到:


















 相關新聞
相關新聞