國內臨床階段的小分子和生物藥統計分析
前言
不久前CDE公布了《2016年度藥品審評報告》,與此同時,CFDA對在中國進行的國際多中心臨床試驗藥物出台新政,旨在縮短新藥在境內外上市的時間間隔。鑒於對國內IND到NDA階段的臨床藥物信息缺乏統計和分析,本文就關注了當前正在國內臨床研發周期內(請注意,不隻是局限於某一年)的藥物相關信息,分別從小分子和生物藥兩個方麵對比闡述。
國內臨床藥物階段統計
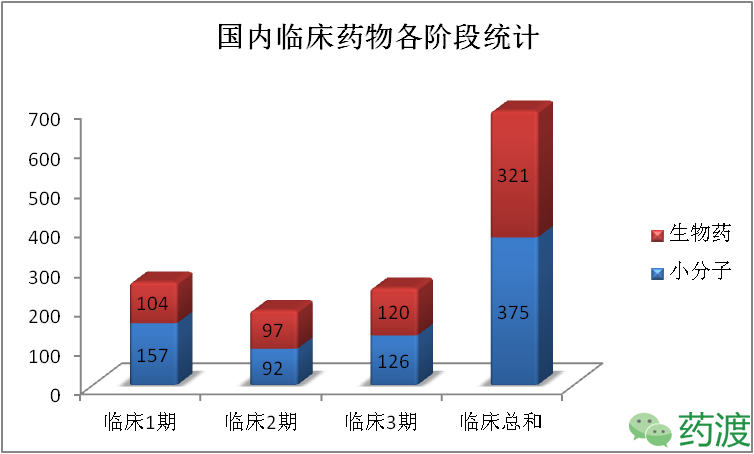
截至2017年3月底,當前國內外各大藥企和研究機構在國內約有700個藥物正在全國各地進行進行臨床試驗(國內CDE已發臨床批件但還未進行臨床試驗的藥物和一致性評價不參與統計),其中小分子包括創新化藥、天然產物、改良製劑、新型組合藥物等;生物藥包括單克隆抗體、多肽多糖、疫苗、抗體偶聯藥物等。當前小分子和生物藥臨床各階段的分布如下圖所示(藥物個數雖然具體,但難免存在偏差,請注意),臨床一期的小分子和生物藥的研發比例為常見的3:2,但臨床二期和三期相應的比例卻約為1:1,主要原因是國內的在研疫苗產品就達60餘個。臨床二期研發的藥物比三期還少,這也體現出二期研發失敗率是1-3期中最高的一個階段。
國內臨床藥物適應症統計
新藥研發的適應症一定程度上也代表著未滿足的臨床需求,雖然CDE年度藥品審評報告中也會對適應症大類進行統計,但顯然不夠具體,本文對國內臨床小分子和生物藥進行適應症方麵的統計則屬於細分領域,如下表所示。
國內臨床小分子適應症排在靠前的主要是腫瘤大類、非小細胞肺癌、肝癌、非胰島素依賴型糖尿病、乳腺癌等,說明國內目前的臨床藥物大多數是針對癌症患者的,且國內的糖尿病、肝病也是臨床試驗的熱點領域。對比臨床生物藥的適應症,我們發現小分子比較青睞的適應症有丙型肝炎病毒感染、阿茲海默症、疼痛等,後兩者是因為生物藥的跨膜障礙,使得生物藥難以在某些疾病領域發揮作用。
國內臨床生物藥的適應症排在靠前的主要是腫瘤大類、類風濕關節炎、乙型肝炎病毒感染、非胰島素依賴型糖尿病、非小細胞肺癌、乳腺癌等。比較特別的是,類風濕關節炎領域的生物藥臨床研究比小分子明顯偏多;另外,在血液疾病領域,如非霍奇金淋巴瘤、彌漫性大B細胞淋巴瘤、嗜中性白血球減少症等是主要傾向於生物藥的。
國內臨床藥物作用機製(靶點)統計
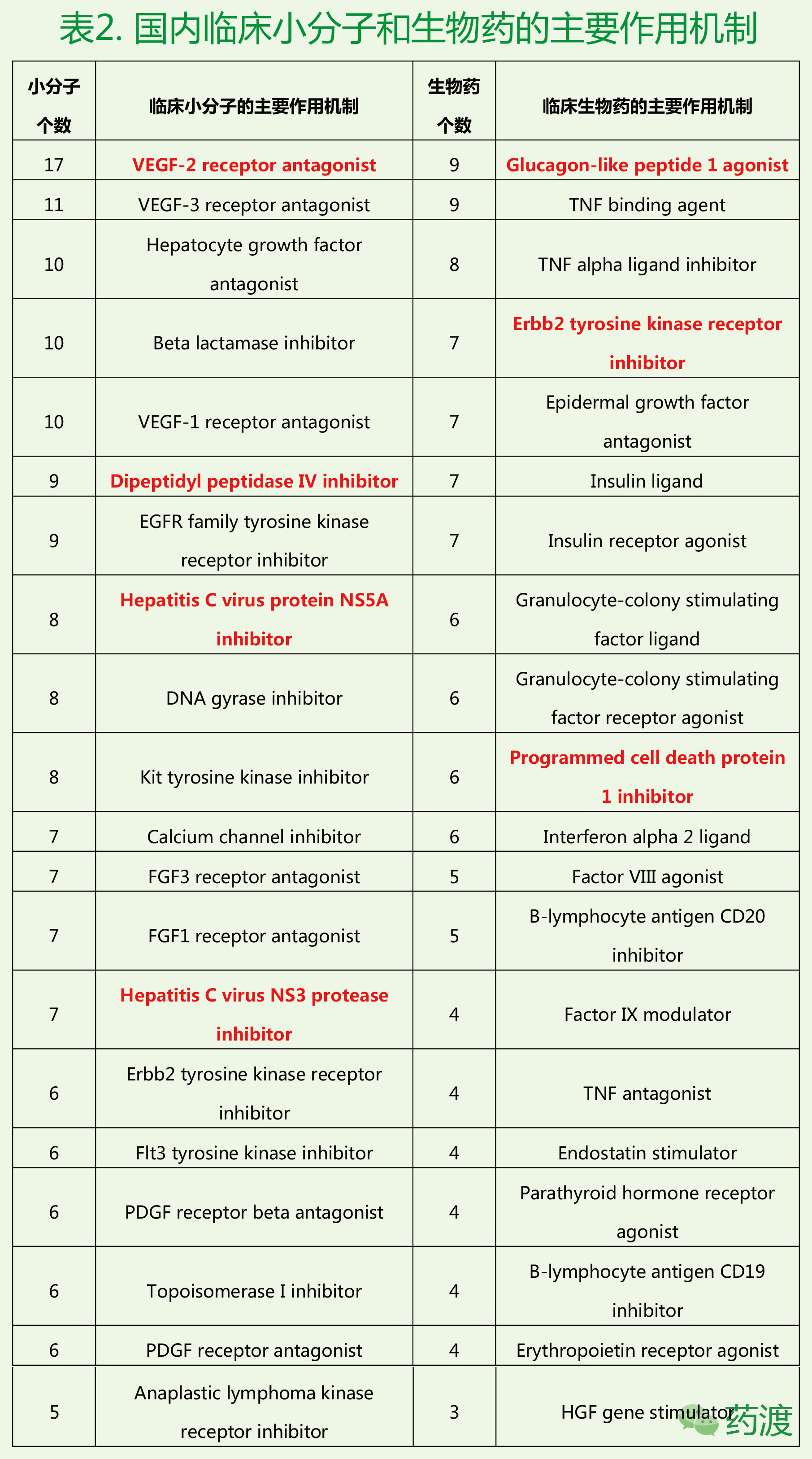
在作用機製(靶點)方麵,近700個國內臨床藥物中暫無明確靶點藥物數達213個,占比約為30%,其中小分子無明確靶點藥物數為107,生物藥無明確靶點藥物數為106。雖然未明確靶點的藥物有許多,但現在靶向藥物的研發依舊是主流,下表列出了國內臨床藥物已有明確靶點的主要作用機製,整體而言,小分子靶向藥的數量要多於生物藥。
國內臨床小分子的靶點主要是Vascular Endothelial Growth Factor (VEGF) Receptor、Dipeptidyl peptidase IV (DPP-4)、HCV NS5A/NS3等,這也與前文所述的適應症相對應,即癌症、糖尿病、肝病。另外抗生素的研發主要針對Beta lactamase和DNA gyrase,也是化學小分子的一大特色。除了7個Calcium channel inhibitor在國內臨床針對心腦血管領域外,其他主要靶點均為癌症/腫瘤領域,如EGFR,Kit,FGF,Erbb2,Flt3,PDGF,ALK等。
國內臨床生物藥的主要作用靶點包括Glucagon-like peptide 1 (GLP-1),Tumor necrosis factor (TNF),Receptor tyrosine-protein kinase Erbb2 (or Her2),Insulin,Insulin Receptor,Granulocyte-colony stimulating factor (GCSF),GCSF Receptor等,其適應症也主要針對腫瘤和糖尿病,除了Erbb2,其餘與國內臨床小分子的主要作用機製有很大不同(從結構生物學角度分析,靶點蛋白表麵和結合位點的特征也使其技術類型偏向生物藥),其中腫瘤免疫療法(如Programmed cell death protein 1 (PD-1) inhibitor,CAR-T CD20/CD19等)在國內臨床也較盛行。
國內臨床藥物企業統計
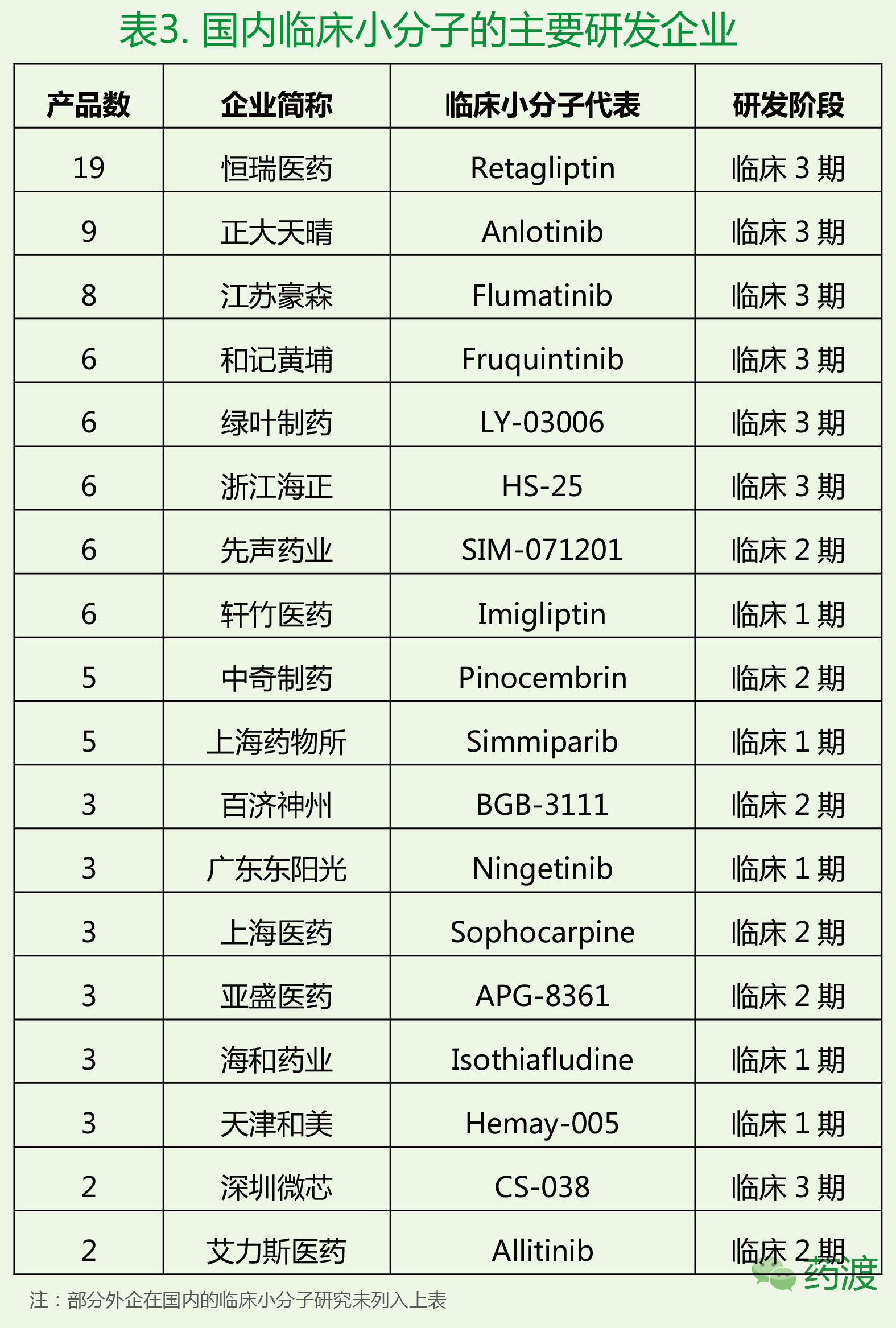
近700個國內臨床藥物涉及的國內外藥企超過200家,其中國內主要藥企在小分子和生物藥的臨床研究情況如下表3和表4所示。
在臨床小分子方麵,國內的恒瑞醫藥可謂一家獨大,擁有眾多創新小分子在臨床1、2、3期研究,正大天晴和江蘇豪森則緊隨其後,其中正大天晴的Anlotinib(安羅替尼)最近已向CDE申報生產。和記黃埔、綠葉製藥、深圳微芯等有相應的產品正處於臨床三期,百濟神州、廣東東陽光、亞盛醫藥等也均具備各自領域的優勢產品。
與臨床小分子相比,臨床生物藥則缺乏研發產品數絕對突出的國內藥企,如下表4所示,西比曼生物、三生製藥、信達生物均擁有自己研發的產品,齊魯製藥、江蘇恒瑞、江蘇豪森等最近幾年也加大對生物藥研發的投入,形成小分子和生物藥的雙重研發戰略。下表也體現出多數藥企專注於生物類似藥(Biosimilar /Biobetter)的研發,這可歸因於未來幾年大量重磅生物藥的專利保護即將到期,生物類似藥將有機會搶占其中一部分醫藥市場份額。
結語
新藥研發不僅在於新,更重要的是其未滿足的臨床需求。最新出台的醫保藥品目錄中,許多國內創新藥紛紛進入醫保,包括其餘正在談判的國內創新藥,這對目前尚處於國內臨床的新藥研發是一大利好。過去十多年來國內上市的創新藥物也就10餘個,最近幾年國內企業對創新藥研發不斷加大投入,有望在新藥研發數量和質量再上一個台階,也真心希望在以後的全球各大重磅藥物預測榜單中,能見到國內企業及其產品的身影!

分享到:
















 相關新聞
相關新聞