
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




5月31日,國家衛計委等部門發布《關於印發首批鼓勵研發申報兒童藥品清單的通知》,清單中列出苯海索等32種藥品的劑型、規格,鼓勵生產企業研發申報,以促進兒童用藥的研發創製。筆者針對清單中32種藥品的上市情況進行統計分析,以方便廣大生產企業了解情況,選擇研發策略。
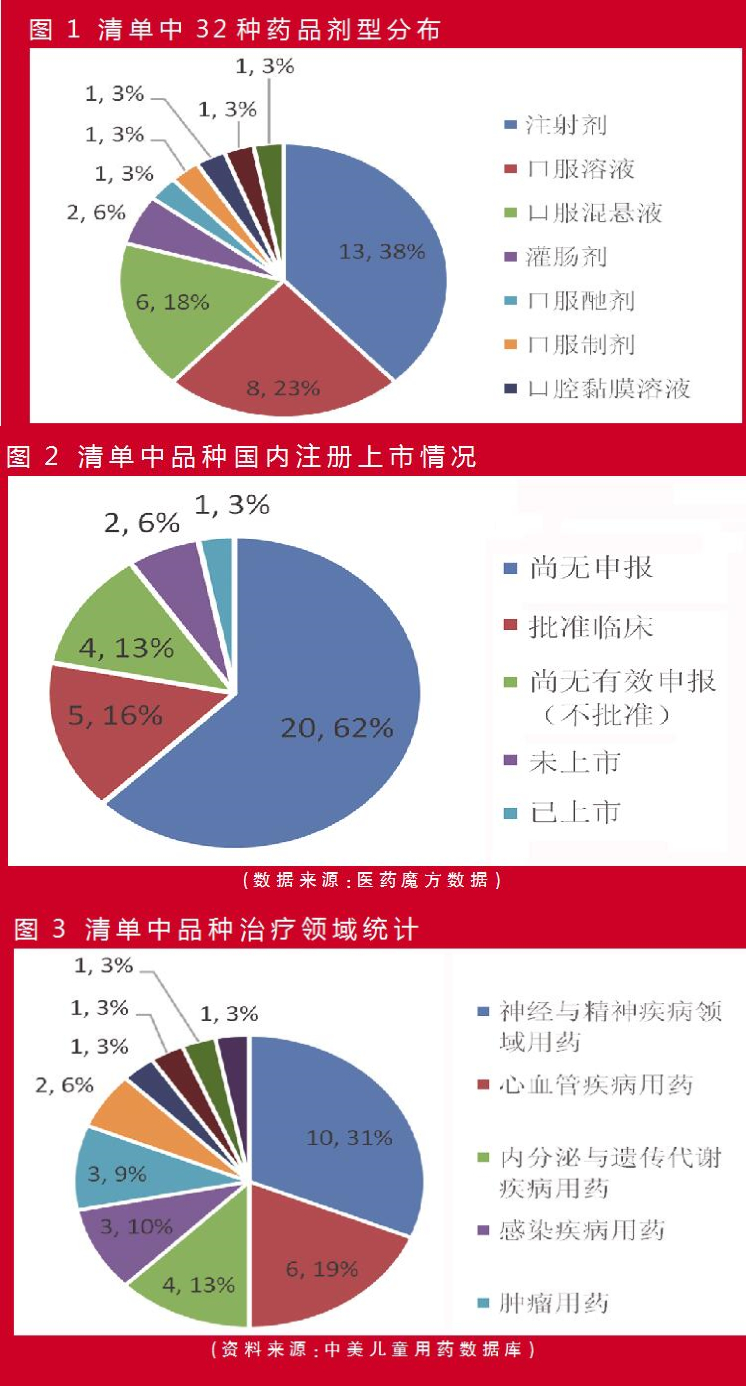
總體情況:目前多數品規未在國內申報,占總數的62.5%
清單中32種藥品的劑型集中在注射劑、口服溶液、口服混懸液等3種兒童適宜劑型(見圖1),占總數的78.12%。實際上,口服酏劑、糖漿劑也屬於口服液體製劑的範疇。口服液體製劑具有“劑量準確、服用方便、依從性好”等優點,因此,在兒童藥品的研發過程中對於口服藥品可以考慮口服液體製劑的開發。
從清單中品規的上市情況來看,目前多數品規尚無申報,占總數的62.5%(見圖2)。
為了解這些品種的國內外市場情況,筆者檢索了美國藥師協會(American Pharmacists Association)視為官方用藥參考指南的《美國兒科劑型手冊》(第21版)(Pediatric & Neonatal Dosage Handbook with International Trade Names Index)和FDA官網數據庫,以及國內兒童用藥主要參考《國家處方集·兒童版2013》,並輔助查找CFDA官網數據庫,以了解這32個品種在美國和我國兒科臨床的使用情況、生產廠家信息以及獲得國內批準文號的情況。
通過檢索發現,清單中32種藥品有25種在國內和美國均有上市;水合氯醛、雙氫睾酮注射劑和凝膠等2個通用名3個劑型品種在我國和美國均無上市信息;苯丙酸氮芥等4種藥品僅在美國有上市藥品,國內暫無已上市的同通用名藥品。
按照藥理作用進行分類,32種藥品主要集中在神經係統與精神類疾病用藥、心血管係統疾病用藥領域,共占50%(見圖3)。
中美共有品種:共涉及25種藥品
【指引】改劑型是研發重點之一,尤其是參考國外兒童藥將現有成人藥品研發成適合兒童使用的劑型和規格。
在25個中美均有上市的品種中,地高辛、腎上腺素、碳酸氫鈉等3個品種的清單推薦劑型已有上市,隻是規格與清單中不一致。
在中美均有上市的25個品種中,有4個品種在國內屬獨家生產:二氮嗪、長春堿在國內隻生產原料藥;促皮質素的原料藥和注射劑由上藥第一生化獨家生產;多粘菌素E、硫酸長春堿注射液均為進口製劑(見表1)。
除上述4個獨家生產品種外,其他21個品種都是有3個及以上多個企業生產的雙信封品種,其中有9個品種國內製劑批準文號已經超過100個。批準文號最多的利福平,有批準文號721個,包括片劑、膠囊劑、注射劑、滴眼液、乳膏、軟膠囊等劑型,但尚無清單推薦的口服混懸液。
從25個品種已上市劑型來看,中國共有54個藥品(不考慮規格),美國共有59種,品種和劑型均一致的有32種,占國內已上市藥品(不考慮規格)總數的59.26%。按照清單上劑型來看,17個藥品的清單上所列劑型在美國已經上市,包括:苯海索口服酏劑、苯妥英鈉注射劑、地高辛注射劑、呋塞米口服溶液、氟呱啶醇口服溶液、勞拉西泮注射劑、尼莫地平口服溶液、普萘洛爾口服溶液、腎上腺素注射劑、碳酸氫鈉注射劑、二氮嗪口服溶液、長春堿注射劑、巰嘌呤口服混懸液、左乙拉西坦注射劑、異煙肼糖漿劑、柳氮磺吡啶、促皮質素注射劑,占共有藥品的68%。
在國內,普萘洛爾、地高辛等藥品已經在成人身上應用多年,安全性和有效性都值得認可,卻沒有兒童的適宜劑型。可見,兒童藥品改劑型是研發的重點之一,尤其是將現有成人藥品研發成適合兒童使用的劑型和規格,參考國外兒童用藥品的劑型和規格,可以為生產企業研發兒童藥品提供參考。
值得注意的是,2016年1月29日,國家藥品審評中心公布第一批優先審評兒童藥品,其中就包括武漢科福新藥有限責任公司的鹽酸普萘洛爾口服溶液(0.5136g:120ml/瓶),與清單中的普萘洛爾口服溶液(1mg/ml)僅規格不同。
美國特有品種:共4種藥品
【指引】了解國外兒科專用藥品臨床試驗和相關專利信息,進行國產仿製藥開發。
有4種藥品雖然在《國家處方集·兒童卷》中未列出,但美國兒科劑型手冊已經對兒童使用進行了介紹(見表2)。其中,FDA於2015年1月批準了重組人甲狀旁腺激素上市,該藥適應症為輔助有甲狀旁腺功能減退症患者對鈣和維生素D吸收,控製低鈣血症。
國內有重慶富進生物醫藥有限公司注冊申報,但尚未被批準。目前雙鷺藥業正在研發,用於治療骨質疏鬆症。由此可見,參考國外兒科用藥品,尤其是療效好、安全性高的兒科專用藥品,了解臨床試驗和相關的專利信息,進行國產仿製藥的開發,也是生產企業進行兒童適宜劑型藥品研發的方向之一。
中美均未上市品種:涉及2個通用名3個劑型品種
水合氯醛和雙氫睾酮(注射劑和凝膠)在我國和美國均無上市。水合氯醛具有鎮靜催眠作用,但由於臨床試驗數據不足可能存在風險而未被FDA和歐盟批準,但在加拿大有上市,國內醫療機構也有自製製劑,但無上市產品。雙氫睾酮是一種雄性激素,用來促進男性第二性征的發育,國內曾有貴陽新天藥業有限公司申報過原料藥和凝膠,但尚未被批準;美國雖無雙氫睾酮,但已有睾酮的注射劑和凝膠,與雙氫睾酮的療效類似。

給兒童藥研發企業的建議
5月18日,國家衛計委等6部委發布《關於加強兒童醫療衛生服務改革與發展的意見》,旨在推動兒童醫療衛生服務體係發展。目前全國約有兒童2.2億人,兒童用藥市場非常龐大。然而,兒童臨床試驗難開展等問題造成我國兒童專科用藥發展緩慢。
此次首批兒童用藥鼓勵研發清單的發布是國內首次以清單形式鼓勵兒童藥品研發生產的政策,無疑是一個進步。在國內兒童藥品適宜劑型缺乏的環境下,鼓勵適宜劑型的開發,有利於保障兒童用藥的可獲得性。針對兒童用藥研發,生產企業可以重點把握以下幾點:
一是針對臨床發展成熟、安全性和有效性高的成人用藥,對比國外兒童用藥,通過改良劑型和規格,研發更加適合兒童使用的劑型和規格。
二是針對國內醫療機構為方便兒科使用而自製的醫院製劑,企業可以考慮進行進一步研發生產上市,該類製劑一般治療效果好,但生產量少、成本較高。
三是針對國外已經上市而國內沒有的兒童用優質原研藥、特效藥,抓緊時間搶仿上市。
 相關新聞
相關新聞