
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




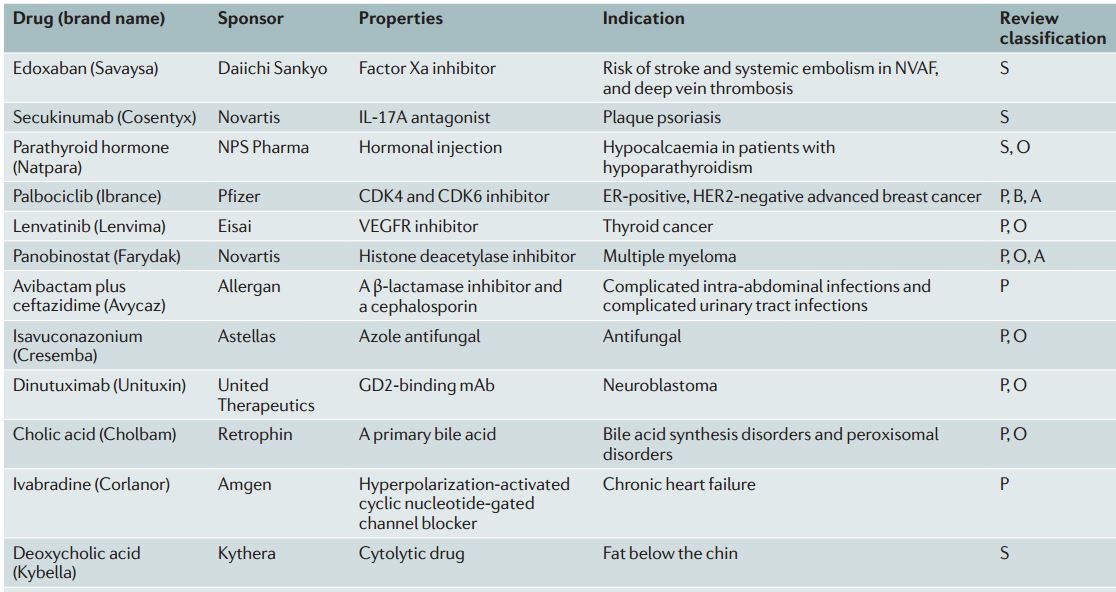
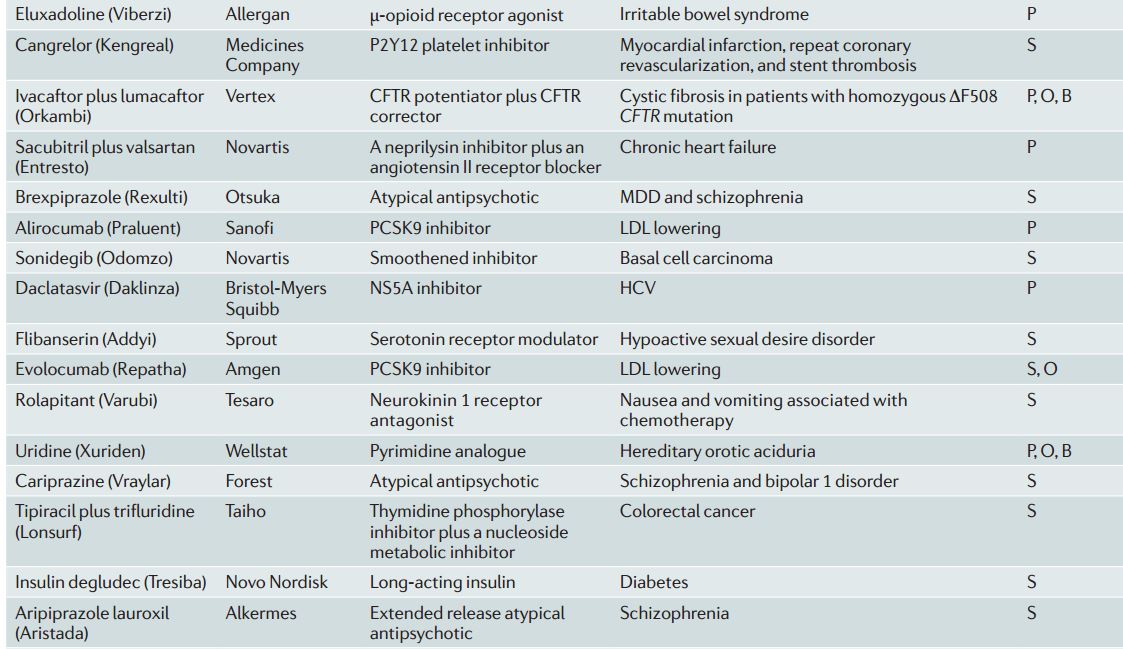
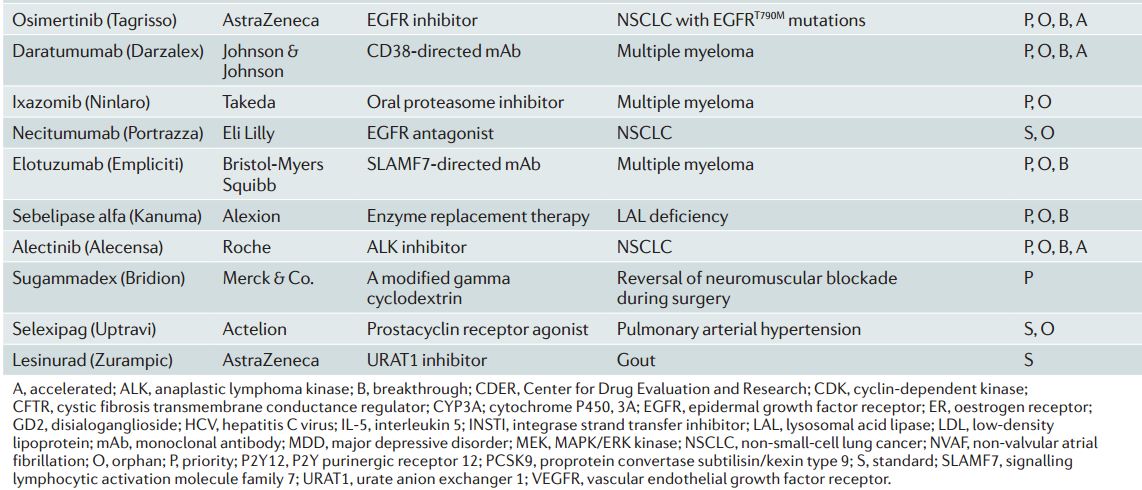
工業界和FDA連續兩年取得了裏程碑式的新藥批準。藥物評估研究中心(CDER,監督小分子和抗體藥物審批)在2015年通過了45種新藥,這是近19年最高的記錄,而且比2014年的41種藥物記錄還要高。(圖1,表1)在2005 -2009年期間(最低點),平均每年隻有22種藥物,2015年要比2005-2009年批準率高2倍以上。
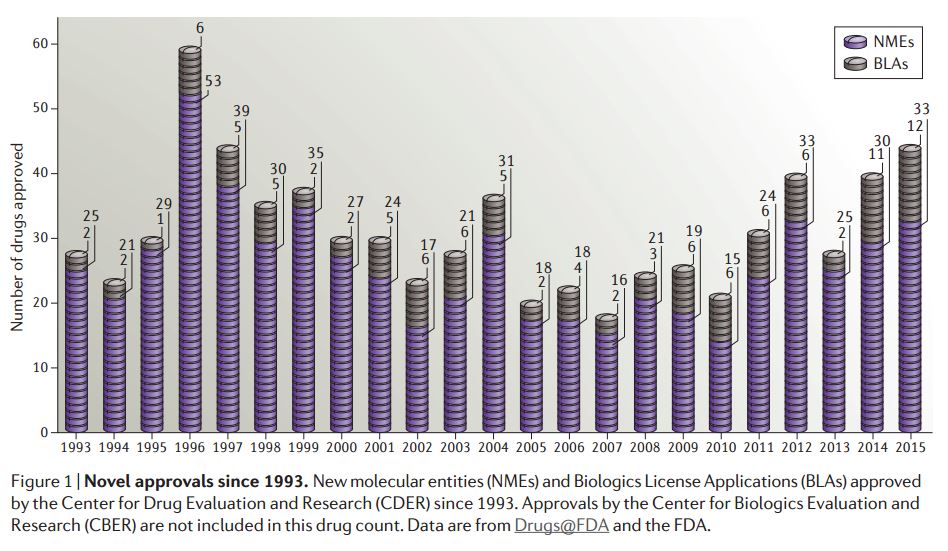
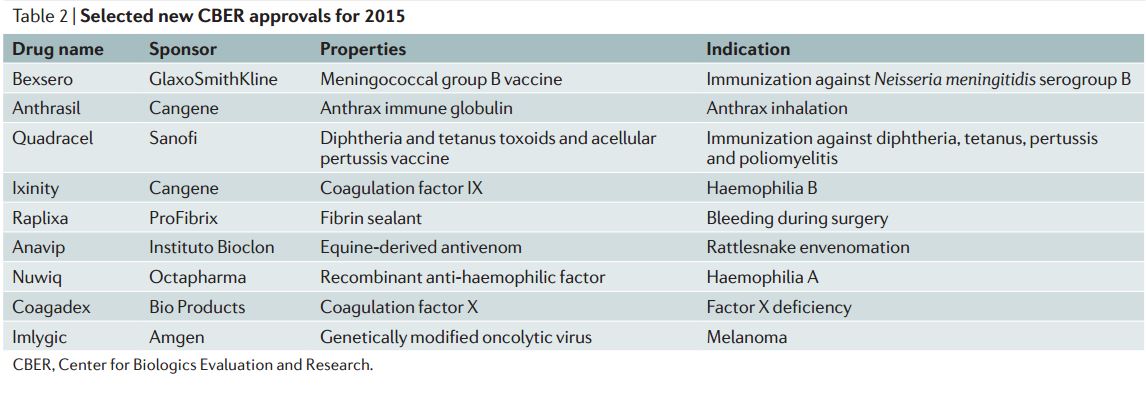
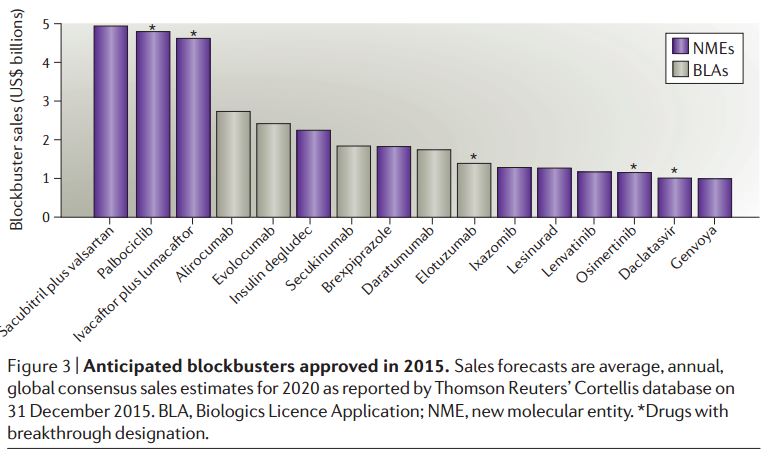
2015年藥物盡管不是很吸引人眼球,但仍然表現出強大的市場潛力。波士頓谘詢團隊對CDEC和CBER(表2)通過的新藥進行每年分析,他們發現2015年批準藥物的平均峰值銷售額會達到9億美元。這個要比2014年的均值---14億美元低,因為2014年FDA批準了Gilead的治療丙肝病毒的銷售記錄保持者--Harvoi聯合治療以及兩種高期望值的免疫抗癌藥。2014年要比2009年平均銷售額高一半。(圖2)
 相關新聞
相關新聞