國內銷售數據和研發數據的公開都很有限,本文盡可能保證可靠的數據來源,但受限於數據來源的限製以及知識儲備的限製,仍然難免出現遺漏和錯誤。歡迎業內朋友補充數據,也歡迎指正文中的數據錯誤,以求建立更準確的國內抗體藥物研發格局。
據CFDA相關老師介紹,截至2015年下半年,共有近200家藥企提交抗體藥物臨床申請,估計國內總計有600家企業在抗體藥物領域布局。考慮到數據獲取的難度,以及研發水平的差異,本文僅針對已經獲得受理並公開的抗體藥物進行分析。
一、CFDA受理的抗體藥物品種
統計範圍說明:統計包括單克隆抗體、抗體片段,VEGF靶點融合蛋白、TNF-α靶點融合蛋白、TNF凋亡誘導配體。
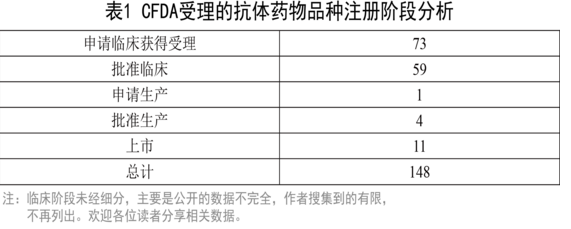
截至2016年03月15日,CFDA公開的受理抗體藥物品種共有280餘個,除去拒絕及重複品種,共有280個。其中進口品種132個,國產品種148個。進口品種多為在歐美等市場已經上市品種,這裏不再詳述,本文針對這148個品種進行具體分析(由於品種過多,這裏不再列出清單)。
147個受理的國產抗體藥物中,研發階段如下:
統計的11個上市藥物如下:
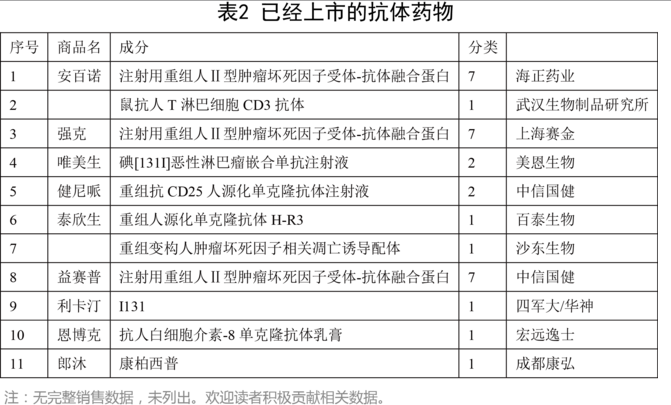
二、企業品種分布
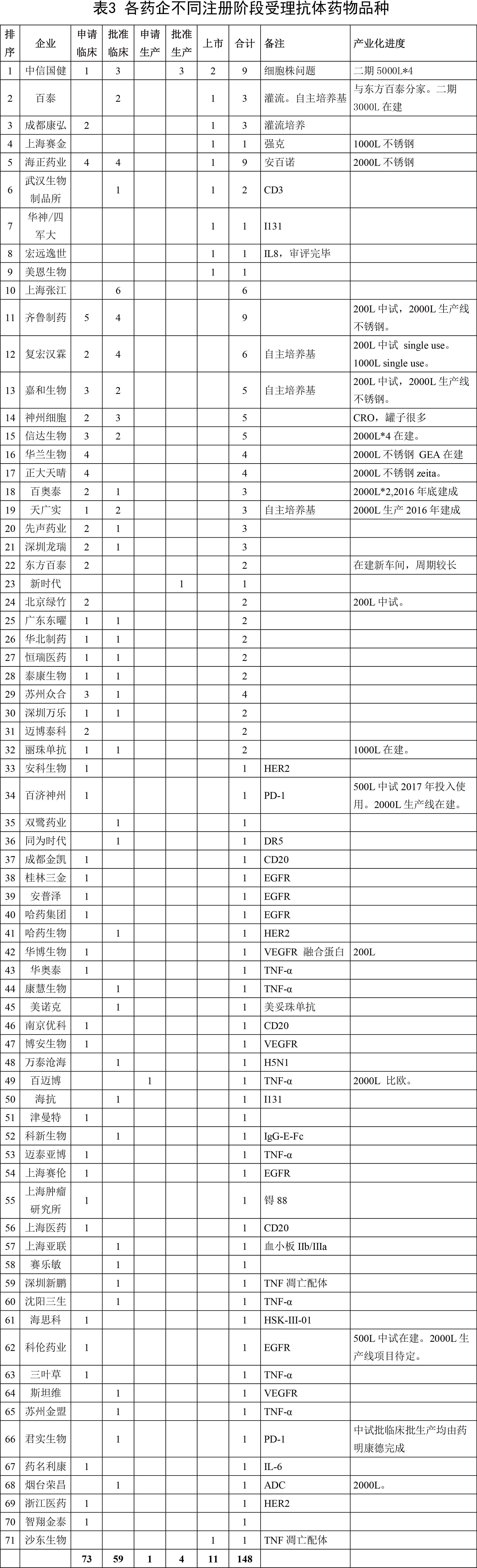
在CFDA公開的已受理147個抗體藥物中,涉及71家藥企,具體分布情況如下表:
從表中可以看出,抗體藥物的研發異常激烈。但尚處於洗牌前階段,各家企業各有長短。且正趕上監管改革的大時代,變數很多,但也意味著後來者仍有機會。抗體研發企業大概可以分為以下幾類:
1. 以中信國健、百泰為代表,國內最早擁有上市抗體藥物產品的生物藥物企業,有研發、生產、營銷的完整產業鏈。但在產業劇烈變革的時代,也麵臨諸多挑戰。
2.以海正藥業、康弘藥業為代表,本身已經具有一定規模的中藥、化藥企業,最早一批重金布局抗體藥物領域的企業。海正在研產品線豐富,但上市產品安百諾營銷壓力大,後續麵臨新一批抗體藥物研發企業的激烈競爭。康弘的郎沐雖上市較晚,但頭頂首個獲得WHO INN的光環,占據了地利人和,獲得了初步成功,後續仍有KH903、KH906等pipeline儲備。但俞德超走後,生物藥長遠如何布局,還要再看;
3.以齊魯製藥、嘉和生物、複宏漢霖為代表,資本充足,起步較晚,以符合國際標準的高質量生物類似藥為突破點來破局。但這類企業也最多,競爭也最為激烈。包括正大天晴、華海藥業等一大批企業;
4.以恒瑞醫藥、百濟神州等為代表,研發水平著眼國際水準,靠自主創新達到核心競爭力。這裏麵又分為兩類,一類是已經擁有雄厚資本的恒瑞藥業,立誌於成為國際一流的創新推動型藥企,一類是百濟神州這種研發型企業,通過資本市場以及合作開發方式,來獲得前期研發需要的資本。這也是歐美通行的研發模式;
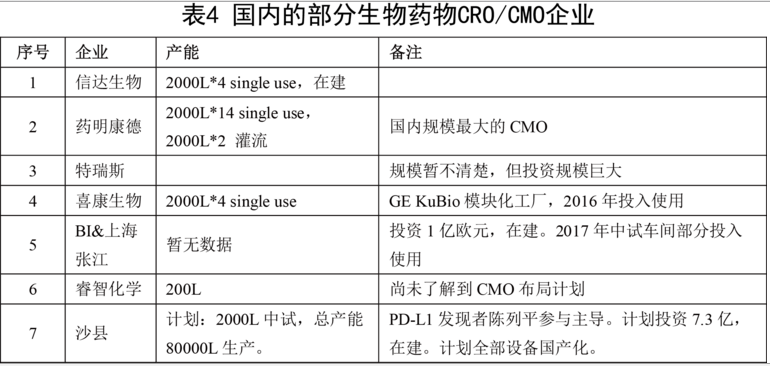
5. 不得不提的還有國內的生物藥物CRO/CMO產業,這類企業在整個抗體藥物發展過程中將發揮巨大作用,甚至影響產業格局。
企業在資本、技術積累、生產能力、疾病譜布局等方麵都存在巨大差異,在製定企業戰略方麵也各有側重。而且今天的國內生物醫藥市場已經不是相對獨立的封閉生態圈,轉而融入到全球生物醫藥發展的大潮,如恒瑞、信達的國際合作開發模式,包括浙江醫藥剛剛獲得受理的ADC藥物,也是和Ambrx合作開發。這一切都是使得競爭格局變得更加複雜,距離成熟的市場格局還要經曆漫長和慘烈的洗牌過程。
三、靶點統計
國內抗體藥物研發以生物類似藥為主,因而靶點也比較集中。除去已經上市了11個抗體藥物,在研的、已受理的137個抗體藥物,靶點以TNF-α、EGFR、VEGF、HER2為主,即全球最暢銷的幾個抗體藥物:Humira、Enbrel、Rituxan、Herceptin、Avastin等為主。這幾個靶點合計的在研抗體藥物數(已受理)為85個,占到總數的75%以上。
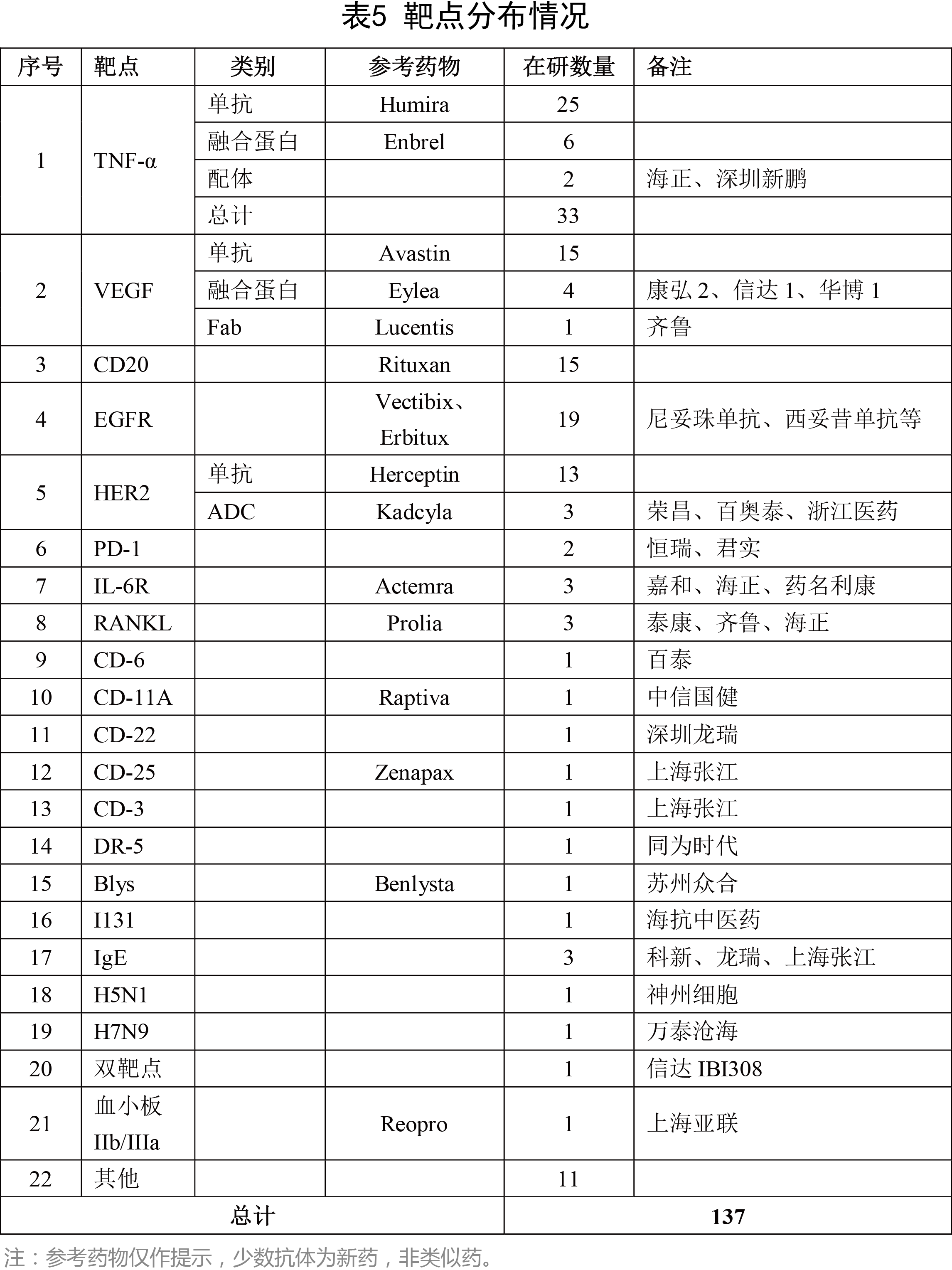
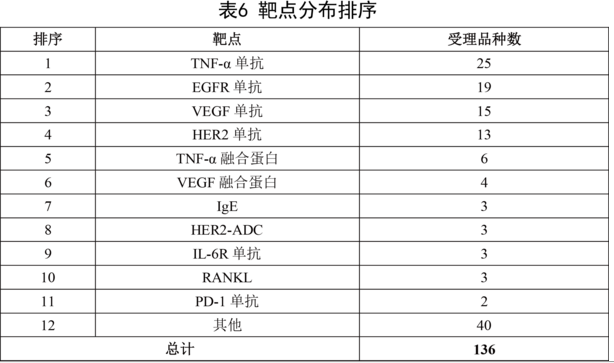
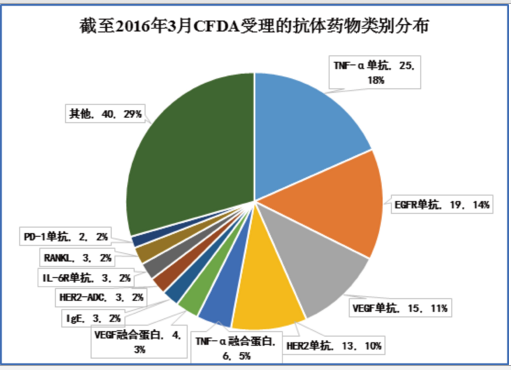
四、抗體類似藥的商業機會
由於目前主要市場中僅歐盟具有相對完善的監管法規體係,並於2014年上市了第一個抗體類似藥Remsima(韓國Celltrion,仿製Remicade)。在此以Remsima為例,分析抗體類似藥的商業機會。
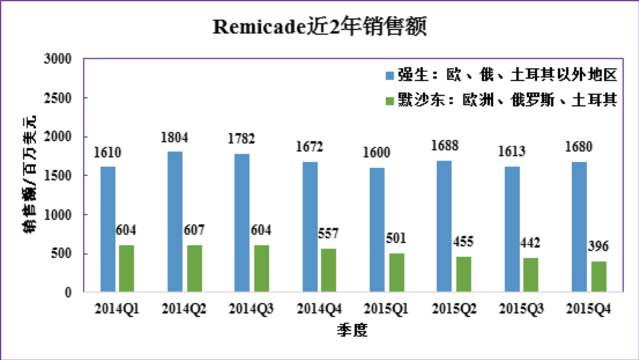
由於歐盟的生物類似藥監管政策體係較為完整,Remicade生物類似藥首先成功登陸歐洲市場,並成為歐美主要市場首個獲批上市的抗體生物類似藥。強生負責的歐洲、俄羅斯、土耳其以外地區的市場並未受生物類似藥影響,銷售額小幅下降4個百分點。反觀默沙東銷售數據,大幅下降四分之一。默沙東在四季報中也承認,Remicade銷售下降主要是歐洲市場上收到生物類似藥的衝擊。
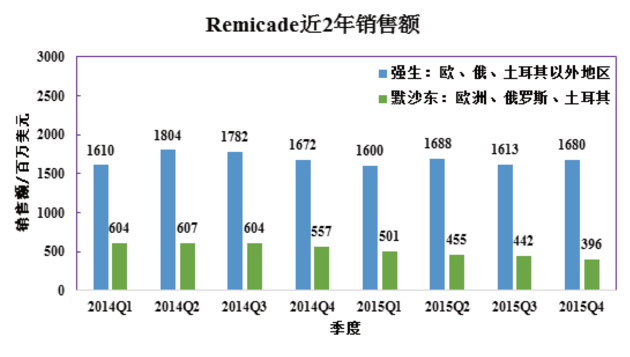
對上述數據進行初步分析,加上類似藥的低價格因素,估計Remsima在歐盟上市第二年實現了3-4億美元的銷售額。這樣的表現,已經算很不錯。這也意味著,抗體類似藥有巨大的商業潛力。
當然,抗體類似藥要想取得成功,還麵臨諸多挑戰。工藝與質量控製的難度、監管對於臨床減免的考量、適應症外推、自由互換等,都將影響抗體類似藥的成本和商業機會。
更重要的還是時間,同時也意味著機會成本,變局來臨,誰都不能漠然對待。




















 相關新聞
相關新聞